سلام
در این مطلب میخواهیم با هم به جمع بندی نکات صفحه 1 تا 23 شیمی دهم (مطابق با آزمون جامع) و خلاصه نکات که برای پاسخگویی به سوالات آزمون باید به آنها مسلط باشید، بپردازیم.
| دانشجوی دکتری تخصصی پیوسته بیوتکنولوژی دانشگاه تهران رتبه 111 منطقه دو - کنکور ریاضی 1394 | |
 | دانشجوی مهندسی عمران دانشگاه تهران رتبه 328 منطقه دو - کنکور ریاضی 1398 |
عنصر های سازنده ی سیاره ها
دو فضا پیمای 1 و 2 در سال 1977 میلادی برای شناخت بیشتر سامانه خورشیدی به فضا فرستاده شدند، وظایف این دو فضا پیما تهیه ی شناسنامه ی فیزیکی و شیمیایی از سیاره ی مشتری، زحل، اورانوس و نپتون که حاوی اطلاعاتی نظیر:
1- نوع عنصر سازنده 2- ترکیب شیمیایی در اتمسفر آنها 3- ترکیب درصد این مواد
مقایسه عناصر موجود در سیاره های مشتری وزمین

تست 1:

تست 2:
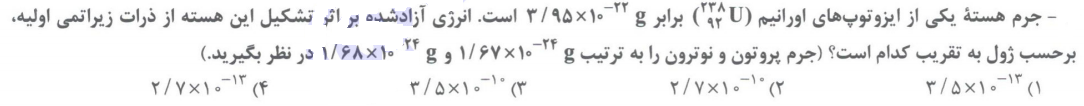
ذره های زیر اتمی، ایزوتوپ
به طور کلی ذره های سازنده ی هر اتم، زیر اتمی نامیده می شوند که مهم ترین آن هاعبارت است از: الکترون، پروتون و نوترون.
عدد اتمی نشان دهنده ی تعداد پروتون های هسته اتم است که با حرف z نشان داده می شود.عددجرمی، نشان دهنده مجموع تعداد پروتون ها و نوترون های هسته اتم است که با حرف Aنشان داده می شود.

برای به دست آوردن تعداد پروتونها و نوترونها در گونه های چند اتمی، کافی است تعداد پروتون ها و نوترون های هر یک از اتمها را با هم جمع کنیم. برای محاسبه تعداد الکترونها در این گونه ها،اگر گونه موردنظر خنثی بود (مثل H2O)،تعداد الکترون ها با تعداد پروتون ها برابر خواهد بود، اما اگر گونه چنداتمی، یون تشریف داشتن ! با توجه به مثبت یا منفی بودن بار آن، به تعداد بار از تعداد پروتون ها کم(برای یونهای مثبت) و یا اضافه برای یون های منفی می شود تا تعداد الکترون ها به دست آید.

ایزوتوپ (هم مکان): به اتم هایی از یک عنصر، که دارای عدد اتمی یکسان و عدد جرمی متفاوتی هستند، گفته می شود.
نکته: ایزوتوپ ها خواص شیمیایی یکسانی دارند ولی برخی خواص فیزیکی وابسته به جرم آن ها مانند چگالی متفاوت است.


نکات:

تست 3:

تست 4:

جدول دوره ای عنصر ها
جدول تناوبی دارای 7 دوره(تناوب) و 18 گروه است.
خواص شیمیایی عنصر هایی که در یک گروه قرار دارد مشابه و خواص عناصر هم دوره متفاوت است. به عنوان مثال هلیم و آرگون متعلق به گروه 18 هستند، تمایل به انجام واکنش ندارند.
با پیمایش هر دوره از چپ به راست، خواص عنصر ها به طور تناوبی و مشابه هم تکرار می شود.
در این جدول، دوره ی اول با 2 عنصر کوتاه ترین و دوره ی6 و 7 با 32 عنصر بلند ترین دوره های جدول دوره ای هستند.
عناصر گروه 18 (گاز های نجیب) تمایلی به انجام واکنش شیمیایی ندارند. یا واکنش پذیری کمی دارند، مثل He, Ar
عناصر گروه 17 (هالوژن ها) یون پایدار با بار منفی را تشکیل می دهند، مانند F, Cl, Br
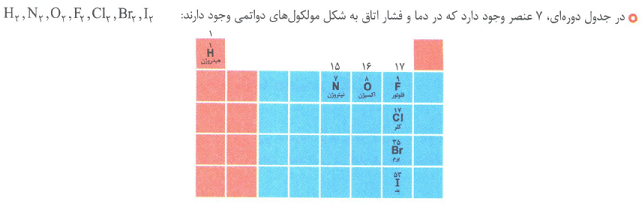
جرم اتمی عنصر ها
دانشمندان برای اندازه گیری جرم اتم ها، از یکای جرم اتمی(amu) استفاده می کنند. جرم هر (amu) معادل 1/12 جرم ایزوتوپ ، «کربن-12» است.
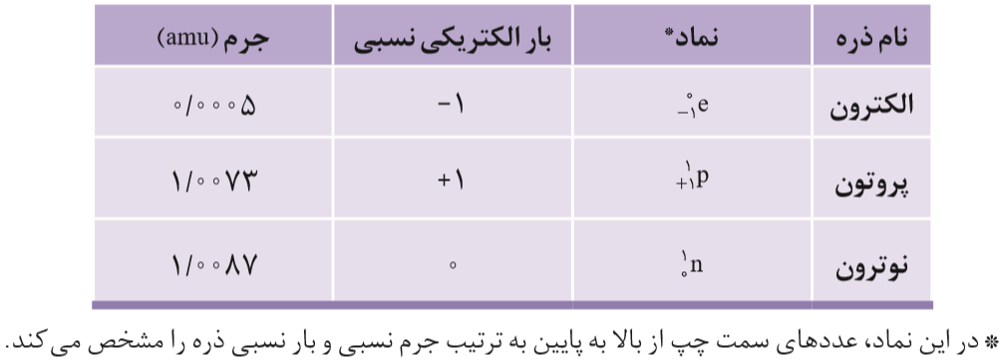
نکته: با توجه به اینکه جرم نسبی پروتون و نوترون حدود amu 1 است می توان گفت، جرم نسبی یک اتم تقریبا معادل با عدد جرمی آن است.
ایستگاه محاسبات:
برای محاسبه ی جرم اتمی میانگین از فرمول زیر استفاده می کنیم:
جرم های ایزوتوپ های عنصر: a1 , a2 , a3 فراوانی ایزوتوپ های عنصر: F1 , F2 , F3
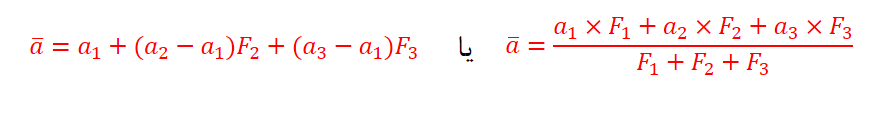
تست 1:
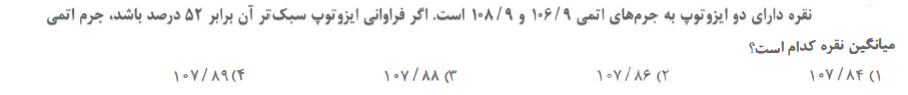
تست 2:

پرتوهای الکترومغناطیس
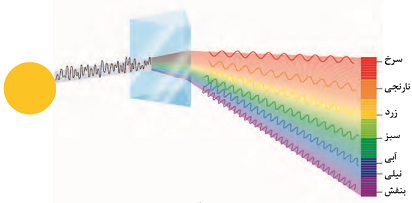
نور: شکلی از انرژی است که به صورت موج منتشر می شود. یکی از ویژگی های موج، طول موج(لاندا) است.
نکته: میزان شکست نور با طولموج رابطه ی عکس دارد، مثلا شکست نور بنفش از نور قرمز بیش است.
چشم انسان یک محدوده ی بسیار کوچک از نور یعنی طول موج 400 – 700 نانومتر را می تواند ببیند که به آن گستره ی مرئی گفته می شود وشامل رنگ های سرخ، نارنجی، زرد، سبز، آبی، نیلی و بنفش است.
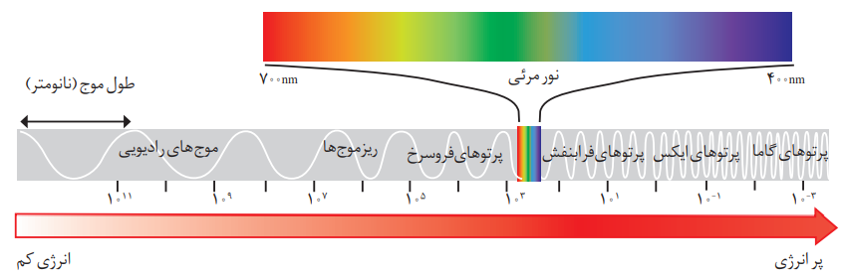
به طور کلی هر چه طول موج پرتویی کوتاه تر باشد،انرژی بیش تری با خود حمل می کند. به عنوان مثال انرژی نور آبی از نور سرخ بیش تراست.
امواج رادیویی < ریز موج ها <فرو سرخ< نور مرئی < فرابنفش < ایکس < گاما : انرژی
طیف نشرخطی عنصرها:
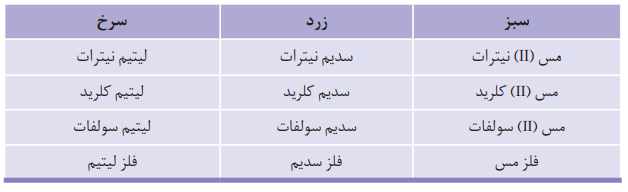
تجربه نشان می دهد که بسیاری از نمک ها، شعله ی رنگی دارند و اگر مقداری از محلول آن ها را روی شعله بپاشیم، رنگ شعله تغییر می کند. رنگ شعله فلزها با رنگ شعله ی ترکیب های دارای این فلزها، مشابه است.
به فرآیندی که در آن یک ماده با جذب انرژی از خود نور (پرتوهای الکترومغناطیس) منتشر می کنند، نشر نور گفته می شود.
اگر نور نشرشده از یک عنصر یا ترکیب دارای آن عنصر را از منشور عبور دهیم، الگویی شامل خط ها یا نوارهای مجزای رنگی به وجود میآید که به آن طيف نشری خطی می گویند.طیف نشری خطی هر عنصر مختص همان عنصر است و می توان از آن برای شناسایی عناصر استفاده کرد.
طیف نشری خطی هیدروژن دارای 4 خط به رنگ های بنفش، آبی، سبز و قرمز می باشد.
نکته:هلیم، لیتیم و نئون به ترتیب دارای 9، 4 و 22 خط در گستره ی مرئی خود می باشند.
مدل کوانتومی اتم:
1- در این مدل اتم مانند کره ای در نظر گرفته می شود که هسته در فضایی بسیار کوچک در مرکز آن قرار دارد.
2- الکترون ها در فضایی بسیار بزرگ تر و در لایه هایی اطرف هسته توزیع می شود.
(لایه ها به ترتیب از طرف هسته به بیرون با شماره های 1، 2 و ... شماره گذاری می شوند.)
3- شماره هر لایه با (n) عدد کوانتومی اصلی، نمایش داده می شود.
4- در ساختار لایه ای، بخش های پررنگ تر، مهم ترین بخش از یک لایه را نشان می دهند که الکترون بیش تر وقت خود را در آن فاصله سپری میکند. (الکترون ها مابقی وقت خود را می توانند در همه ی نقاط پیرامون هسته حضور داشته باشند.)
5- در این مدل، داد و ستد انرژی به صورت کوانتومی صورت می گیرد. یعنی الکترون هنگام انتقال از یک لایه به لایه دیگر انرژی را به صورت پیمانه ای یا بسته ای جذب یا نشر می کند.
توجه : کوانتومی بودن داد و ستد انرژی به معنای « پله پله بودن » آن است. یعنی الکترون نمی تواند به هنگام بالا رفتن و پایین آمدن از لایه ها در هر جایی قرار بگیرد و فقط می تواند بر روی لایه قرار گیرد، آن هم با جذب و یا نشر مقدار انرژی معین و کافی!!
نکته: از آن جا که انرژی داد و ستد شده هنگام انتقال الکترون ها کوانتومی است، ساختار لایه ای اتم را مدل کوانتومی نیز نامیده اند.
نکته: هر چه میزان انرژی جذب شده بیش تر باشد، الکترون به لایه های بالاتر می رود و به هنگام بازگشت انرژی بیشتری آزاد می کند.
نکته: هرچه به هسته نزدیک تر شویم، تفاوت انرژی بین دو لایه ی متوالی افزایش می یابد.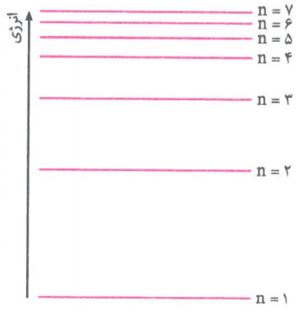
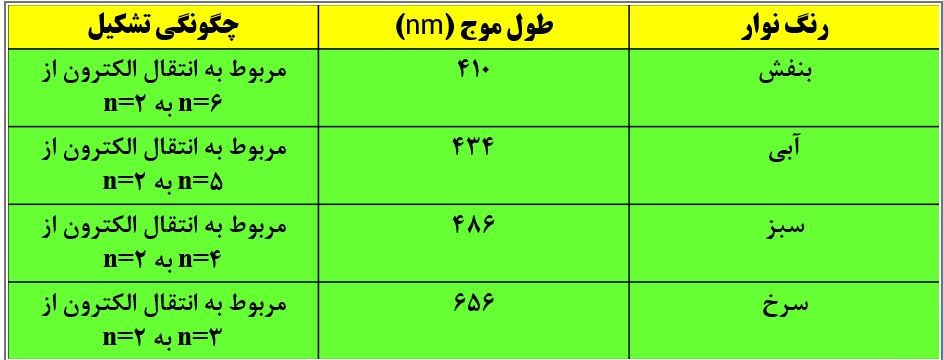
طیف نشری خطی هیدروژن
در گستره ی مرئی طیف نشری خطی به دست آمده از اتم های هیدروژن،چهار خط یا نوار رنگی وجود دارد. این خطوط مربوط به انتقال الکترون از لایه های بالاتر (n=3,4,5,6) به لایه ی دوم (n=2) هستند.
تست :

تست :

دوستان عزیز می توانید برای دسترسی به نسخه کامل خلاصه نکات به همراه پاسخ فایل پی دی اف زیر را دانلود کنید!
فراموش نکنید اگر سوالی در رابطه با این مبحث داشتید می توانید به راحتی در کامنت ها سوال خود را برای ما بنویسید.
دوستان عزیزم؛ برای ارتباط با رتبه برترها صفحه اینستاگرام زیر رو دنبال کنید.


