توجه:
شما با مطالعه این درسنامه می توانید به سوالات 641-660 و 721-740از کتاب نوروز و سوالات 91،614،772،925،1072،1232از کتاب زرد پاسخ دهید.
برای خرید کتاب ها به سایت کانون بوک مراجعه کنید.
دانش آموزان عزیز سلام
در این مطلب قصد داریم نکات مباحث ابتدایی فصل یک شیمی دوازدهم را به همراه سوالات نهایی و کنکور در اختیار شما قرار دهیم تا آمادگی لازم را کسب کنید .
 | رویا خواجوی رتبه 8 منطقه سه ، کنکور تجربی 1403 دانشجوی دندانپزشکی شهید بهشتی |
درسنامه شامل :
خلاصه مطالب و نکات
5 تست کنکور سال های اخیر
سوالات نهایی مربوطه
در ابتدا سوالات نهایی مرتبط با مبحث را بررسی می کنیم .

• شوینده ها براساس خواص اسیدی و بازی عمل میکنند.
• وبا یک بیماری واگیردار است که به دلیل آلوده شدن آب و نبود بهداشت شایع میشود.
ساده ترین و مؤثرترین راه پیشگیری این بیماری، رعایت بهداشت فردی و همگانی است.
• شاخص امید به زندگی نشان میدهد با توجه به خطراتی که انسانها در طول زندگی با آن مواجه هستند، به طور میانگین چند سال در این جهان زندگی میکنند .
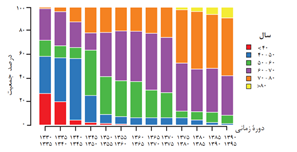
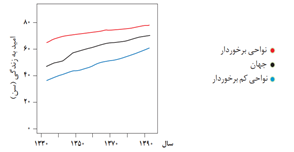
• شاخص امید به زندگی در نواحی برخوردار بیشتر از نواحی کم برخوردار و شیب منحنی برای نواحی کم برخوردار بیشتر از میانگین جهانی و آن نیز بیشتر از مناطق برخوردار است همچنین شاخص امید به زندگی در حال حاضر به طور میانگین 65 سال است .
• آلاینده ها موادی هستند که بیش از مقدار طبیعی در یک محیط، نمونه ماده یا یک جسم وجود دارند.
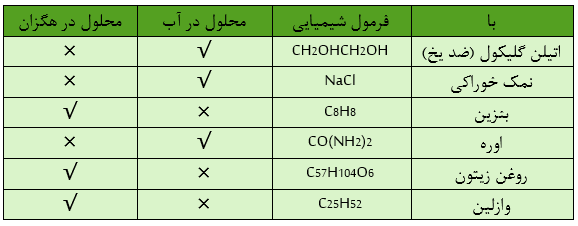
• اتیلن گلیکول و اوره قابلیت تشکیل پیوند هیدروژنی بین مولکول های خود و همچنین با آب هستند .
• روغن زیتون استر سه عاملی و سیر نشده است .
• در فرایند انحلال، اگر ذره های سازنده حل شونده با مولکول های حلال جاذبه های مناسب برقرار کنند، حل شونده در حلال حل میشود در غیر این صورت ذره های حل شونده کنار هم باقی می مانند و در حلال پخش نمی شوند. هنگامی که عسل وارد آب می شود، مولکول های سازنده آن با مولکول های آب پیوند هیدروژنی برقرار می کنند و در سرتاسر آن پخش می شوند.
• چربی ها را می توان مخلوطی از اسیدهای چرب 1و استرهای بلند زنجیر (با جرم مولی زیاد) دانست ، اسیدهای چرب، کربوکسیلیک اسید هایی با زنجیر بلند کربنی هستند .
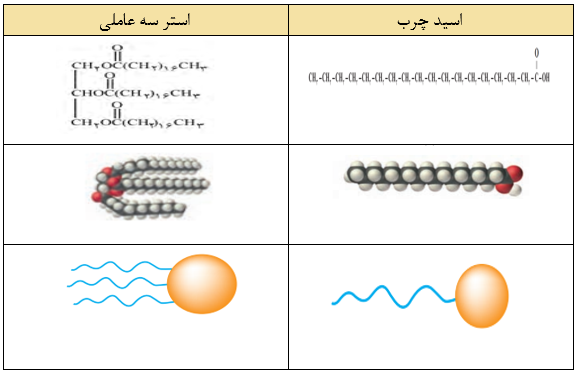
فرمول کلی اسید های چرب : CnH2nO6
فرمول مولکولی اسید چرب سازنده استر سه عاملی : C3H2)÷3-فرمول مولکولی استر)
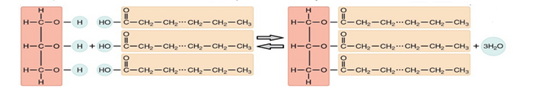
• نیروی بین مولکولی غالب در چربی از نوع واندروالسی است . و به دلیل ناقطبی بودن در آب نا محلول اند .
•صابون را میتوان نمک سدیم اسید چرب دانست. فرمول همگانی این نوع صابون ها که جامد هستند، RCOONaبوده که در آن Rیک زنجیر هیدروکربنی بلند است.

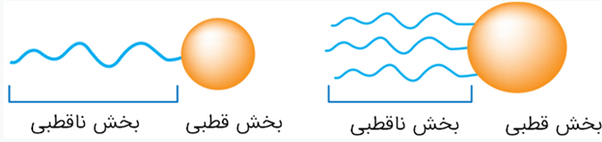
•هر گاه مخلوط مقداری از این صابون و آب را هم بزنید، مولکول های صابون در سرتاسر مخلوط پخش میشوند چون صابون از طریق بخش قطبی آنیون خود پیوند یون دو قطبی با مولکول های آب برقرار می کند بنابراین در آب حل می شوند .
•صابون جامد را از گرم کردن مخلوط روغن های گوناگون یا چربی مانند روغن زیتون، نارگیل و پیه با سدیم هیدروکسید تهیه میکنند. صابون های مایع، نمک پتاسیم یا آمونیوم اسیدهای چرب هستند .
فرمول صابون مایع (نمک پتاسیم) : CnH2n+1COOK
فرمول صابون مایع (آمونیوم اسید چرب) : CnH2n+1COONH4
فرمول صابون جامد : CnH2n+1COONa
• تشکیل صابون از استر سه عاملی:
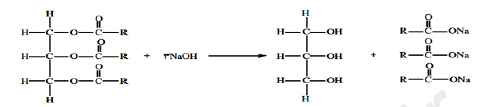
• اغلب موادی که در زندگی روزانه با آنها سروکار داریم، از مخلوط دو یا چند ماده تشکیل شده اند.
•کلوئید ها مخلوط هایی به ظاهر همگن اند که حاوی توده های مولکولی با اندازه های متفاوت و ناهمگن می باشند .
• ذره های موجود در کلوئید درشت تر از محلولاند و به همین دلیل نور را پخش میکنند .
• رفتار کلوئیدها را میتوان رفتاری بین سوسپانسیون و محلول ها در نظر گرفت .
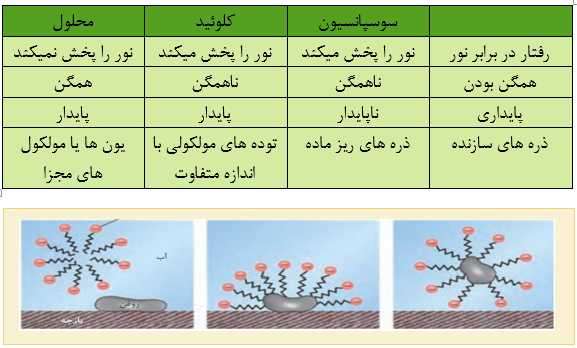
• هنگامی که صابون وارد آب میشود، به کمک سر آب دوست خود در آن حل میشود. از سوی دیگر، ذره های صابون با بخش چربی دوست خود با مولکول های چربی جاذبه برقرار میکنند، گویی مولکول های صابون مانند پلی بین مولکول های آب و چربی قرار میگیرند. به این ترتیب، ذره های چربی کم کم از سطح پارچه جدا و در آب پخش میشوند. با ادامه این فرایند، همه لکه های چربی از روی لباس پاک میشود.
• نوع پارچه، دما، نوع آب و نیز نوع و مقدار صابون بر روی قدرت پاک کنندگی آن تأثیر دارد . 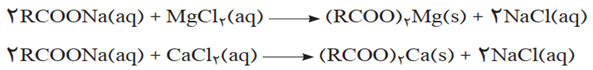
• با انجام واکنش های شیمیایی بالا و تشکیل رسوب در آب سخت که دارای مقادیر چشمگیری از یون های کلسیم و منیزیم می باشد قدرت پاک کنندگی صابون کاهی می یابد ، لکه های سفیدی که پس از شستن لباس با صابون روی آنها برجای می ماند، نشانه ای از تشکیل چنین رسوب هایی است .
• افزایش دما و افزودن آنزیم میزان پاک کنندگی صابون را افزایش می دهد . و میزان چسبندگی لکه های چربی روی پارچه های مختلف یکسان نیست و به میزان قطبیت پارچه بستگی دارد بنابراین میزان قطبیت پارچه نخی بیشتر از استری است .
• چالش تولید صابون به روش سنتی تامین چربی بسیار زیاد بود همچنین صابون در همه شرایط به خوبی عمل نمی کرد . زیرا استفاده از آن در محیط های گوناگون مانند سفرهای دریایی و صنایع وابسته به آب شور، پاسخگوی نیاز انسان نبود .
• شیمی دان ها در جستوجوی موادی بودند که قدرت پاک کنندگی زیادی داشته باشند و بتوان آنها را به میزان انبوه و با قیمت مناسب تولید کرد. با توجه به رابطه بین ساختار و رفتار یک ماده، شیمی دان ها به دنبال تولید موادی بودند که ساختار آن ها شبیه صابون باشد. آنها توانستند از بنزن و دیگر مواد اولیه در صنایع پتروشیمی، پاک کننده هایی که به پاک کننده های غیر صابونی مشهور اند بسازند .
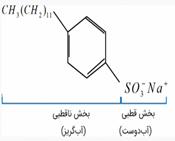
• مقایسه پاک کننده های صابونی و غیر صابونی :
پاک کننده های غیر صابونی بر خلاف صابون که از واکنش ساده بین چربی و سود سوز آور به دست می آید از مواد پتروشیمیایی و طی واکنش های پیچیده ای تولید می شود . بخش آبدوست شوینده های صابونی و غیر صابونی با یکدیگر متفاوت است . پاک کننده های غیر صابونی بر خلاف صابونی دارای حلقه بنزنی می باشند . پاک کننده های غیر صابونی چون با کاتیون های موجود در آب سخت واکنش نمی دهند قدرت پاک کنندگی بیشتری نسبت به صابون دارند . در هر دوی این پاک کننده ها نسبت کاتیون به آنیون برابر یک و هر دو یونی اند . هر دوی پاک کننده ها هم در چربی هم در آب محلول اند . مکانیسم هر دو برای پاک کردن لکه های چربیاز طریق بر همکنش است نه واکنش . عوارض جانبی پاک کننده غیر صابونی بیشتر است .
• از نوعی صابون سنتی در تنور نان سنگک برای چرب کردن سطح سنگ ها استفاده میشود.
•صابون طبیعی معروف به صابون مراغه بیش از 150سال قدمت دارد . این صابون افزودنی شیمیایی ندارد و به دلیل خاصیت بازی مناسب برای موهای چرب استفاده میشود.
• صابون گوگرددار، برای از بین بردن جوش صورت و همچنین قارچ های پوستی استفاده میشود. همچنین به منظور افزایش خاصیت ضدعفونی کنندگی و میکروب کشی صابون ها به آنها ماده شیمیایی کلردار اضافه میکنند. از سوی دیگر برای افزایش قدرت پاک کنندگی مواد شوینده، به آنها نمک های فسفات می افزایند، زیرا این نمک ها با یون های کلسیم و منیزیم موجود در آب های سخت واکنش می دهند و از تشکیل رسوب و ایجاد لکه جلوگیری میکنند. هر چه شوینده های مواد شیمیایی بیشتری داشته باشد، احتمال ایجاد عوارض جانبی آن بیشتر خواهد بود. مصرف زیاد شوینده ها و تنفس بخار آنها، عوارض پوستی و بیماری های تنفسی ایجاد میکند.
• پاک کننده های خورنده پاک کننده هایی هستند که از نظر شیمیایی فعال اند و خاصیت خورندگی دارند. به همین دلیل نباید با پوست تماس داشته باشند . این پاک کننده ها می توانند با آلاینده ها واکنش شیمیایی بدهند و آنها را به فراورده هایی تبدیل کنند که با آب شسته شوند .

• نوعی پاک کننده که به شکل پودر عرضه میشود شامل مخلوط سدیم هیدروکسید و پودر آلومینیم است. این پاک کننده برای باز کردن مجاری مسدود شده در برخی وسایل و دستگاه های صنعتی استفاده میشود .

•سدیم هیدروکسید موجود در مخلوط با بخشی از چربی ها یا اسید های چرب موجود در مجاری واکنش داده و باعث تولید صابون میشود که به سهولت زدودن آلاینده ها می انجامد . تولید گاز H2 باعث تلاطم بیشتر محلول و برخورد شدیدتر ذره ها با یکدیگر می شود و حباب های ریز و پر فشار گاز ضربات متعدد و پی در پی به آلاینده ها وارد و جدا شدن آنها از سطح لوله را تسهیل میکند و باعث میشود چربی ها ذوب شده و از مسیر زدوده می شود . ویژگی گرماده بودن این واکنش دما را شدیدا بالا می برد تا جایی که آب جوش می آید و آب جوش در مقایسه با آب معمولی توانایی بیشتری برای زدودن آلاینده ها دارد همچنین باعث می شود چربی ها ذوب شوند و از سطح لوله ها پاک شوند .
• اسیدهای خوراکی مزه ترش و بازها مزه تلخ دارند. اسیدها با اغلب فلزها واکنش می دهند و در تماس با پوست سوزش ایجاد می کنند. در حالی که بازها در سطح پوست همانند صابون، احساس لیزی ایجاد می کنند اما به آن نیز آسیب میرسانند .
• یاخته های دیواره معده با ورود مواد غذایی به آن هیدروکلریک اسید ترشح میکنند. این اسید افزون بر فعال کردن آنزیم ها برای تجزیه مواد غذایی، جانداران ذره بینی موجود در غذا را نیز از بین می برد .

• پیش از آنکه ساختار اسیدها و بازها شناخته شود، شیمی دان ها افزون بر ویژگی های اسیدها و بازها با برخی واکنش های آنها نیز آشنا بودند. سوانت آرنیوس نخستین کسی بود که اسیدها و بازها را بر یک مبنای علمی توصیف کرد. او بر روی رسانایی الکتریکی محلول های آبی کار میکرد. یافته های تجربی او نشان داد که محلول اسیدها و بازها رسانای برق هستند، هر چند میزان رسانایی آنها با یکدیگر یکسان نیست .
• ماده ای که در آب سبب افزایش غلظت یون هیدرونیوم می شود اسید آرنیوس و ماده ای که در آب سبب افزایش یون هیدروکسید می شود باز آرنیوس نامیده می شود . هرچه [+H ] در محلولی بیشتر باشد، آن محلول اسیدی تر و هر چه [- OH]در محلولی بیشتر باشد، آن محلول بازی تر است. اگر در یک سامانه غلظت یون های هیدرونیوم و هیدروکسید با هم برابر باشد، آن سامانه حالت خنثی دارد .

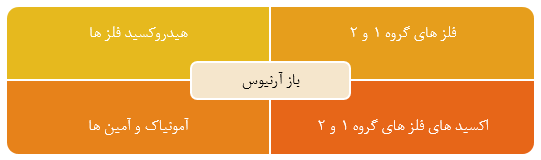
• ترکیب هالوژن با هیدروژن قبل حل شدن در آب یک ترکیب مولکولی گازی شکل و هیدروژن نامیده می شود و اما با ورود به آب یونیده می شود و هیدرو هالیک اسید نامیده می شود .
• دی نیتروژن پنتااکسید و لیتیم اکسید و باریم اکسید در دمای اتاق جامد اند . و گوگرد تری اکسید حالت گازی دارد .
• NOو N2Oو COبه طور فیزیکی در آب حل می شوند و یون هیدروژن را افزایش نمی دهند بنابراین اکسید اسیدی نیستند .
• با مدل آرنیوس میتوان اسید و باز را تشخیص داد اما نمیتوان درباره میزان اسیدی یا بازی بودن یك محلول اظهار نظر كرد .
سوالات نهایی و کنکور متناسب با مطلب را در فایل پی دی اف مطالعه کنید .


