دانش آموزان عزیز سلام💖
در این مطلب قصد داریم نکات فصل دو شیمی دهم را به همراه سوالات نهایی و کنکور در اختیار شما قرار دهیم تا آمادگی لازم را برای آزمون پیش رو کسب کنید. فایل پی دی اف شامل سوالات نهایی و کنکور را در انتهای مطلب مشاهده می کنید.
| موازنه و پایستگی جرم فصل دو شیمی دهم خلاصه نکات و تست | رویا خواجوی رتبه 8 منطقه 3 کنکور تجربی 1403 دانشجوی دندان پزشکی دانشگاه شهید بهشتی |

- «در ابتدا برای درک اهمیت این مبحث سوالاتی که در امتحان نهایی دهم آورده شده را باهم بررسی میکنیم. بعد از خواندن درسنامه سعی کنید به سوالات پاسخ بدهید و بعد جوابتان را با پاسخنامه فایل ضمیمه مقایسه کنید.»
- ⭕نمودار زیر مربوط به تغییر دمای یك گلخانه در یك روز زمستانی است.
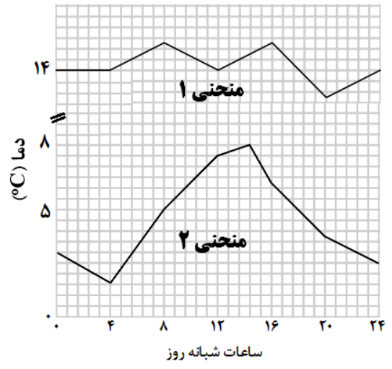
- آ) کدام منحنی مربوط به درون گلخانه است؟ چرا؟
ب) نام یا فرمول شیمیایی یك گاز گلخانه ای را بنویسید.
- ⭕در مجتمع فولاد مباركه اصفهان براي استخراج آهن از واكنش زير استفاده ميشود:
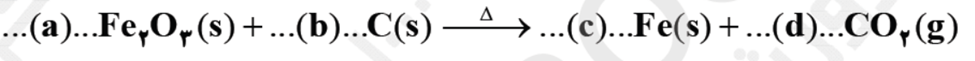
الف) با موازنه واکنش a، b، c و d را در معادله واکنش تعیین کنید.
ب) آرایش الکترونی کامل Fe را بنویسید.
ج)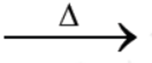 درواكنش به چه معناست؟
درواكنش به چه معناست؟
- ⭕با توجه به واکنش های داده شده، به پرسش ها پاسخ دهید.
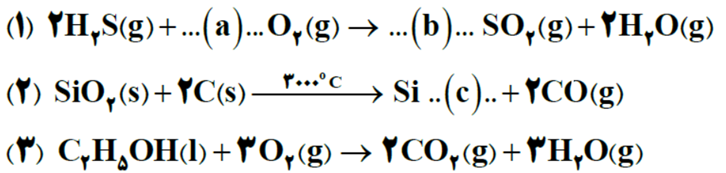
الف) در واکنش1 ضرایب a و b را تعیین کنید.
ب) نماد در واکنش 2 بیانگر چیست؟
پ) در واکنش 2 سیلیسیم به حالت مذاب تشکیل می شود. نماد مناسب آن را به جای (c) بنویسید.
ت) واکنش3 کدام نوع سوختن (ناقص یا کامل) را نشان می دهد؟ چرا؟
واکنش شیمیایی
هر تغییر شیمیایی می تواند شامل یك یا چند واکنش شیمیایی باشد، تغییر شیمیایی می تواند با تغییر رنگ، مزه، بو یا آزاد سازی گاز، تشکیل رسوب و گاهی ایجاد نور و صدا همراه باشد.
كه هر یك از واکنش ها را با یك معادله نشان می دهند. در این معادله، واكنش دهنده ها در سمت چپ و فراورده ها در سمت راست نوشته می شوند.
🔸مثال: سوختن کربن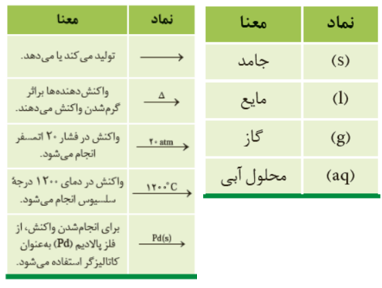
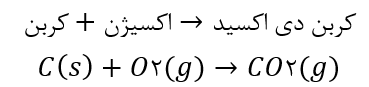
معادلۀ نخست، نوشتاری و معادلۀ دوم، نمادی نامیده می شود. معادلۀ نمادی، افزون بر نمایش فرمول شیمیایی واكنش دهنده ها و فراورده ها می تواند حالت فیزیکی آنها و اطلاعاتی دربارۀ شرایط واكنش نیز ارائه کند.
❗در معادلۀ واکنش، رسوب حالت جامد، مذاب حالت مایع و بخار حالت گاز دارد.
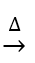 تنها به این معنا است که واکنش دهنده ها بر اثر گرما واکنش می دهند (ربطی به گرماگیر یا گرماده بودن واکنش ندارد)، واکنش هایی وجود دارند که برای شروع آنها نیاز به گرما است و این واکنش می تواند گرماگیر یا گرماده باشد.
تنها به این معنا است که واکنش دهنده ها بر اثر گرما واکنش می دهند (ربطی به گرماگیر یا گرماده بودن واکنش ندارد)، واکنش هایی وجود دارند که برای شروع آنها نیاز به گرما است و این واکنش می تواند گرماگیر یا گرماده باشد.
پایستگی جرم
در واكنش های شیمیایی، اتمی از بین نمی رود و به وجود هم نمی آید، بلكه پس از انجام واكنش، اتم های واكنش دهنده ها به شیوه های دیگری به هم متصل می شوند و فراورده ها را به وجود می آورند. این ویژگی نشان می دهد كه جرم مواد، پیش از واكنش برابر با جرم مواد، پس از واكنش است؛ به دیگر سخن، جرم مواد شركت كننده در یك واكنش شیمیایی، ثابت است. مطابق قانون پایستگی جرم، شمار اتم های هر عنصر در یك واكنش شیمیایی ثابت است (شمار اتم ها ثابت است اما تعداد مول یا مولکول های دو طرف واکنش لزوما برابر نیستند). جرم كل مواد موجود در مخلوط واكنش ثابت است.
❗در زنگ زدن میخ آهنی جرم میخ افزایش می یابد، جرم اضافه شده به میخ مربوط به جذب اکسیژن و رطوبت هوا می باشد. در واقع مجموع جرم میخ و اکسیژن و رطوبت جذب شده برابر با جرم میخ زنگ زده است.
موازنه كردن معادلۀ واكنش های شیمیایی
برای موازنه كردن هر معادلۀ نمادی، باید برای هر یك از واكنش دهنده ها و فراورده ها ضریبی قرارداد تا شمار اتم های هر عنصر در دو سوی معادله برابر شود. براساس یکی از ساده ترین روش های موازنه (روش وارسی) اغلب به ترکیبی که دارای بیشترین شمار اتم است؛ ضریب ١ می دهند سپس با توجه به شمار اتم های این ترکیب، ضرایبی را به دیگر مواد می دهند تا شمار اتم های هر عنصر در دو سوی معادله برابر شود. البته در معادله های شیمیایی موازنه شده، نیازی به نوشتن ضریب ١ نیست. توجه به این نکته ضروری است که هریک از ضریب ها در معادلۀ موازنه شده، باید کوچک ترین عدد طبیعی ممکن باشد.
به هنگام موازنه نباید زیروند های واکنش دهنده ها و فراورده ها را تغییر دهیم.
اگر با روش وارسی به بن بست خوردیم باید به موادی که ضرایب آنها معلوم نیست، یک ضریب مجهول مثلا a، b و.. بدهیم و با نوشتن موازنه اتم ها بر حسب این این ضرایب معادله هایی را به دست می آوریم و موازنه را انجام می دهیم.
ویژگی های یک معادله موازنه شده:
- 🔷فرمول شیمیایی مواد به درستی نوشته شده باشد.
- 🔷حالت فیزیکی مواد به درستی مشخص شده باشد.
- 🔷مجموع تعداد اتم های هر عنصر در دو سمت معادله یکسان باشد.
- 🔷ضرایب، کوچکترین عدد طبیعی ممکن باشد.
- 🔷از ضرایب کسری استفاده نشده باشد.
چه بر سر هواکره می آوریم؟
سبك زندگی انسان، نوع وسایلی كه در زندگی استفاده می كند و رفتارهایی كه در شرایط مختلف محیطی انجام می دهد، روی هواكره تأثیر می گذارد؛ سبك زندگی می تواند بیانگر میزان اثرگذاری هر یك از انسان ها بر كرۀ زمین و هواكره باشد.
ردپا اصطلاحی است كه به این اثر نسبت داده اند. یكی از این ردپاها، ردپای كربن دی اكسید است. ردپای کربن دی اکسید نشان می دهد در تولید یك محصول یا بر اثر انجام یك فعالیت چه مقدار از این گاز تولید و وارد هواکره می شود. برای اینكه مقدار كربن دی اكسید در هواكره از مقدار طبیعی آن فراتر نرود، باید مقدار اضافی کربن دی اکسید به وسیلۀ گیاهان یا دیگر پدیده های طبیعی مصرف شود. حال هر چه مقدار كربن دی اكسید وارد شده به طبیعت زیادتر باشد، ردپای ایجاد شده سنگین تر و اثر آن ماندگارتر خواهد بود؛ زیرا زمان لازم برای تعدیل این اثر به وسیله پدیده های طبیعی طولانی تر است. یک درخت تنومند سالانه در حدود 50 کیلوگرم کربن دی اکسید مصرف می کند. با افزایش قطر درخت تاثیر آن در کاهش کربن دی اکسید افزایش می یابد.
➰ردپای CO2: زغال سنگ ˂ نفت خام ˂ گاز طبیعی ˂ انرژی خورشید ˂ گرمای زمین ˂ باد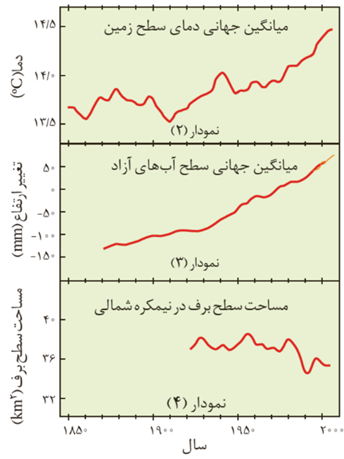
🛑در اثر سوزاندن سوخت های فسیلی، انواع آلاینده ها از جمله CO، CO2، SO2، NO2، CxHy وارد هوا كره می شود.
🛑افزایش مقدار کربن دی اکسید باعث افزایش میانگین دمای کره زمین شده است به طوری که از شال 1850 تا 2000 دمای زمین به طور میانگین از 7/13 به 4/14 رسیده است.
🛑افزایش مقدار کربن دی اکسید و به دنبال آن افزایش دمای زمین موجب ذوب شدن یخ های قطبی شده و سطح آب اقیانوس ها و دریاها بالا آمده است و از طرف دیگر موجب کاهش میانگین برف در نیمکره شمالی شده.
🛑به دلیل گرم شدن زمین و کوتاه شدن زمستان، فصل بهار در نیمکره شمالی نسبت به 50 سال گذشته حدود یک هفته زودتر آغاز می شود.
🛑كربن دی اكسیدی كه وارد هواكره شده، در آن جابه جا می شود و می تواند هوای شهرهای دیگر را نیز آلوده كند. بنابراین هر رفتار ما بر زندگی همه مردمان جهان اثرخواهد گذاشت.
🛑هوای آلوده بوی بدی دارد و چهره شهر را زشت می كند. این هوا باعث سوزش چشم، سردرد، تهوع و به وجود آمدن انواع بیماری های تنفسی مانند سرطان ریه می شود.
اثر گلخانه ای
گلخانه ها، زمین های کشاورزی ویژه ای هستند که دور تا دور آنها را تا ارتفاع معینی با لایه ای از پلاستیک های شفاف می پوشانند. و در آنها گیاهان و میوه های گوناگونی پرورش می دهند. گلخانه، گیاه یا میوه را از آسیب های ناشی از تغییر دما و آفت ها حفظ می کند.
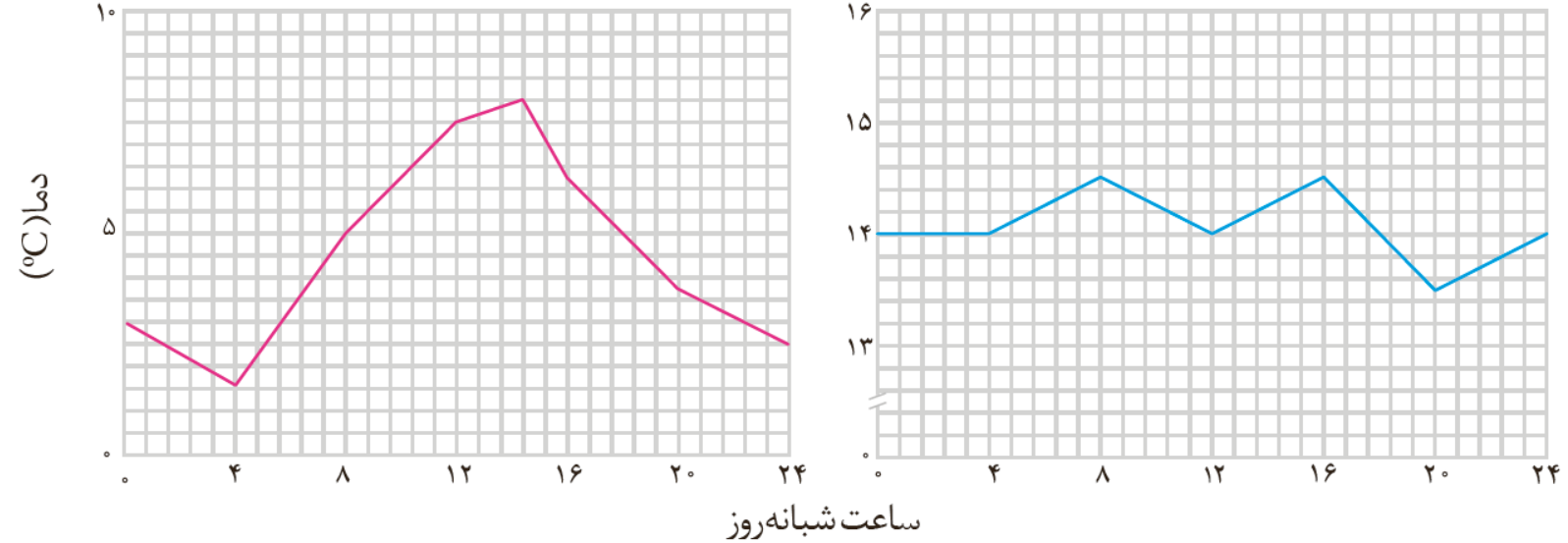
💠تغییرات دمای بیرون گلخانه بیشتر از تغییرات دمای درون گلخانه است همچنین میانگین دمای درون گلخانه بالاتر است.
💠تعداد دفعات تغییر دمای درون گلخانه بیشتر می باشد اما شدن تغییرات بسیار کمتر است.
💠پایین ترین دمای درون گلخانه بیشتر از بالاترین دمای بیرون آن است.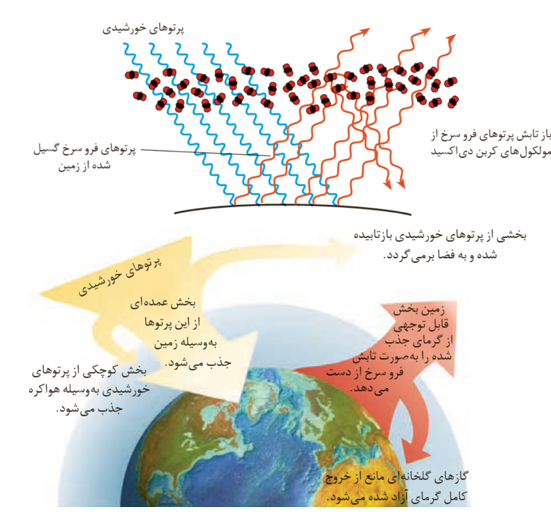
نور خورشید هنگام گذر از هواكره با مولكول ها و دیگر ذره های آن برخورد میكند و تنها بخشی از آن به سطح زمین می رسد. از این رو، زمین گرم می شود و مانند یك جسم داغ از خود پرتوهای الكترومغناطیس گسیل می دارد؛ با این تفاوت كه انرژی پرتوهای گسیل شده، كمتر و طول موج آنها بلندتر است. کرۀ زمین با لایه ای از گازها به نام هواکره احاطه شده است. این لایه برای زمین همانند لایۀ پلاستیکی برای گلخانه است و سبب گرم شدن کرۀ زمین می شود به طوری که اگر این لایه وجود نداشت میانگین دمای کرۀ زمین به -18 درجه سانتی گراد کاهش می یافت. با این توصیف پرتوهای خورشیدی پس از برخورد به زمین دوباره با طول موج های بلندتر (بیشتر از نوع فروسرخ) به هواکره بر می گردند اما برخی گازهای موجود در هواکره مانند CO2 و H2O مانع خروج آنها می شوند و بدین ترتیب زمین را گرم تر می کنند. هرچه مقدار این گازها در هواکره بیشتر باشد، دمای زمین بالاتر خواهد رفت.
با توجه به تصویر گاز های گلخانه ای بخش عمده پرتو های خورشیدی و همچنین پرتو های گسیل شده را عبور می دهند.
- سوالات کنکور:
- ⭕ضریب استوکیومتری کدام ماده، پس از موازنه معادله واکنش: CaSiO3(s)+HF(aq)→CaF2(aq)+SiF4(g)+H2O، بیشتر است؟
1)H2O 2)CaSiO3 3)HF 4)CaF2
- ⭕پس از موازنه واکنش ها، نسبت مجموع ضرایب استوکیومتری واکنش دهنده ها در واکنش (ll) به مجموع ضرایب استوکیومتری فراورده ها در واکنش (l) کدام است؟
(l) NH2CH2COOH(l)+O2→CO2(g)+N2(g)+H2O(g)
(ll) Fe(s)+H2O(l)+O2(g)→Fe(OH)3(s)
1)55/0 2)65/0 3)60/0 4)70/0
- ⭕چند مورد از مطالب زیر، درست است؟
در مولکول HCN، کربن، اتم مرکزی به شمار می آید.
در واکنش های تشکیل سولفوریک اسید و نیتریک اسید، مواد گازی شکل، شرکت دارند.
در واکنش اکسیژن با فلز هایی مانند منیزیم و نافلز هایی مانند گوگرد، انرژی می تواند به صورت نور و گرما آزاد شود.
در یک واکنش مشخص، برای جلوگیری از انجام واکنش های جانبی ناخواسته، استفاده از جو نیتروژن نسبت به جو اکسیژن مناسب تر است.
1)1 2)2 3)3 4)4


