سلام به همه هشتمی های عزیز 🖐🖐
در این مطلب به فصل سوم کتاب علوم هشتم میپردازیم.

🔴ویژگیهای مطلب🔴
درسنامه کامل و نکات
مثال های فراوان
پاسخ کلیدی و تشریحی در فایل ضمیمه
🔴از درون اتم چه خبر🔴
| تاریخچه بوجود آمدن جدول تناوبی عناصر نخستین کسی که در مورد جدول تناوبی توانست نظر بدهد شیمیدان آلمانی بنام یوهان ولفگانگ دوبراینر بود که عناصر را بدون اطلاع از ساختار درونی شان کنار هم قرار داد به دنبال او شیمیدان انگلیسی جان نیولندز عناصر را با توجه به فاصله هشت تایی عناصر از نوع مشابه را به نت های موسیقی شبیه نمود که مورد مسخره معاصرین خود قرار گرفت. سرانجام دو شیمیدان بنام لوتار مایر آلمانی و دیمتری ایوانوویچ مندلیف روسی تقریبا بطور هم زمان اولین جدول تناوبی را با توجه به جرمشان در جدول قرار دادند. | 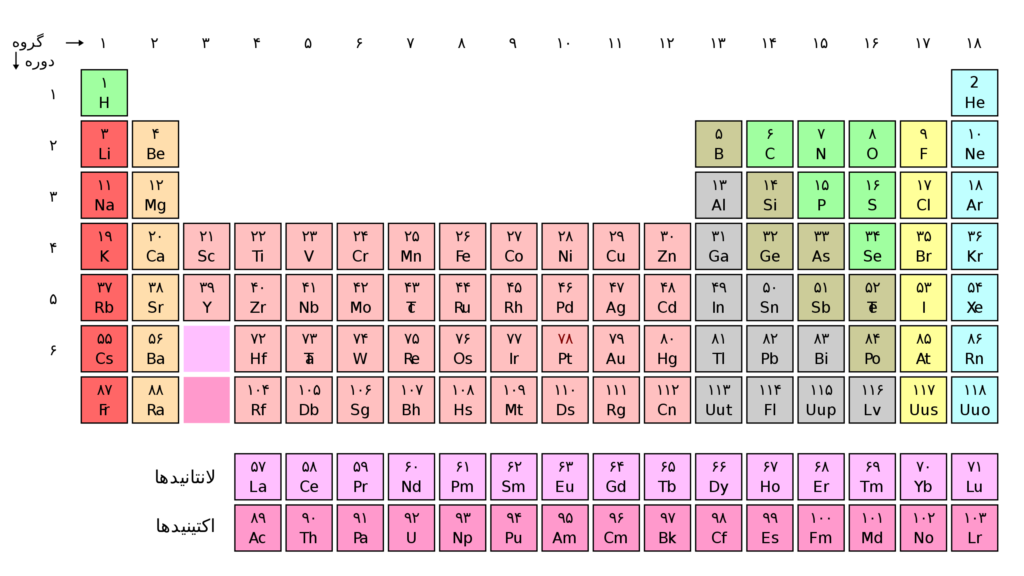 |
زندگینامه دیمتری ایوانوویچ مندلیف : (۱۹۰۷-۱۸۳۴ ) معلم شیمی در سال ۱۸۷۱م اهل روسیه بنام دیمتری ایوانوویچ مندلیف به حصلت تناوبی عنصرهایی برد. او عناصر را با توجه به افزایش جرم اتمی در جدولی قرارداد اما بعضی از عناصر که خواص مشابه داشتند طبق جرم اتمی قرار نمی گرفتند این مشکل جدول مندلیف بود تا اینکه ۴۰ سال بعد دانشمندی انگلیسی بنام هنری موزلی ( ۱۹۱۵-۱۸۸۷) عناصر را با توجه به عدداتمی شان یعنی تعداد پروتون ها مرتب کرد و جدول مندلیف را اصلاح نمود. |  |
انواع ذره های سازنده اتم عبارتنداز: الف) الكترون:
ب) پروتون
ج) نوترون
| 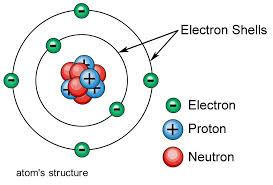 |
نکته: اتم در حالت عادی خنثی ( بدون بار الکتریکی ) است یعنی تعداد الکترون ها بار منفی و پروتون های بار مثبت آن برابر است. | 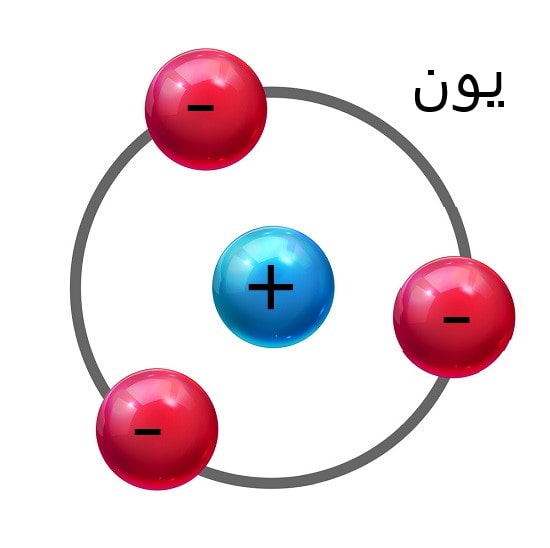 |
عدداتمی چیست؟ مجموع تعداد پروتون های موجود در هسته یک اتم است که با حرف z نمایش می دهند.
با تغییر تعداد پروتون ها نوع اتم نیز تغییر می کند. برای مثال عدد اتمی کربن برابر ۶ و عدد اتمی هیدروژن برابر ۱ است. نتیجه می گیریم که هر اتم کربن ۶ پروتون و هر اتم هیدروژن یک پروتون دارد. | 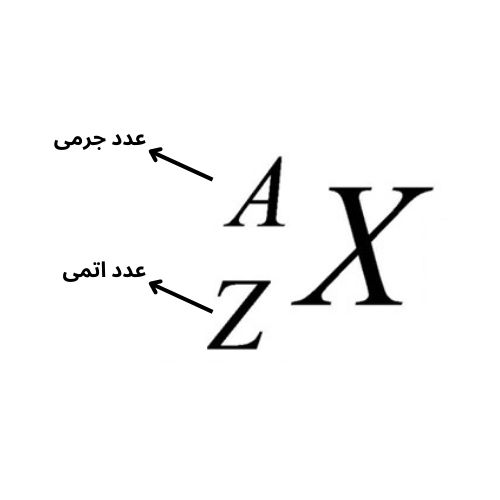 |
عدد جرمی چیست؟ مجموع تعداد پروتون ها و نوترون های موجود در هسته یک اتم است که با حرف A نمایش می دهند. | 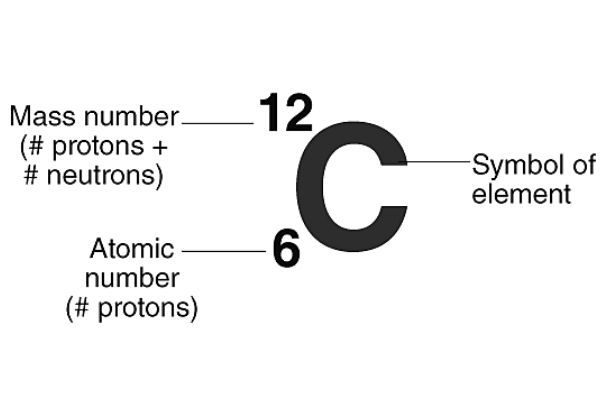 |
ساده ترین اتم در طبیعت چیست؟ هیدروژن است که با حرف H نمایش داده می شود و عدداتمی یک دارد. |  |
- نماد شیمیایی چیست؟
یک یا دو حرف از نام لاتین (انگلیسی) یک عنصر را نماد شیمیایی آن عنصر می گویند.

مکان نوشتن عدد اتمی عدد جرمی در نماد شیمیایی عناصر : |  |
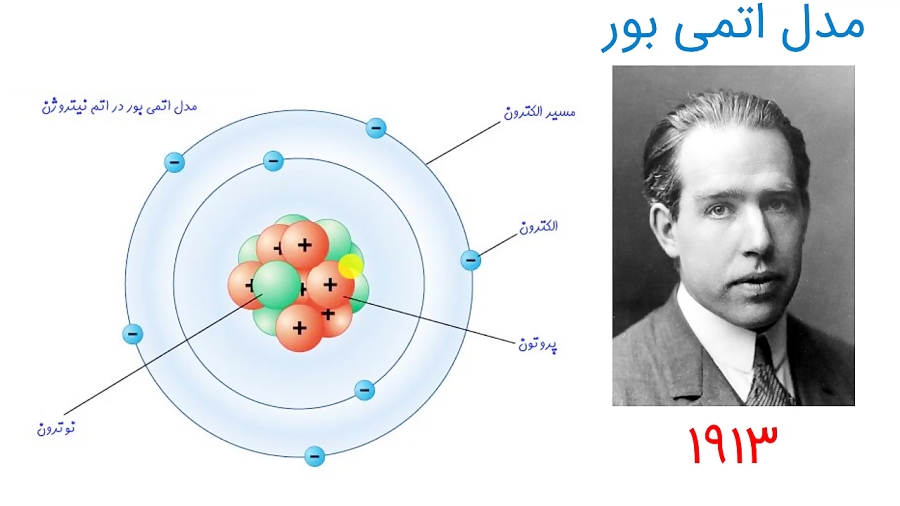
مدل اتمی بور و زندگینامه: ( ۱۹۶۲، ۱۸۸۵) نیلز هنریک دیویدیوهر در هفتم اکتبر ۱۸۸۵ میلادی در کپنهاک دانمارک به دنیا آمد. پدرش بنام کریستیان بور استاد فیزیولوژی دانشگاه کپنهاک بود. در سال ۱۹۰۳ در رشته فیزیک دانشگاه کپنهاک نام نویسی کرد. در مورد آزمایش کشش سطحی آب و اندازه گیری نیروی آن برتر از بقیه دانشجویان شد. در نوامبر ۱۹۲۲ از طرف فرهنگستان علوم سوئد جایزه نوبل به نیلز بور داده شد. در دهه ۱۹۳۰ بر روی نظر به فیزیک کوانتومی هسته ای نقش داشت. در ۱۸ نوامبر ۱۹۶۲ در کینهاک در سن ۷۷ سالگی در گذشت. در سال ۱۹۱۳ میلادی فیزیکدان دانمارکی بنام نیلز هنريك ديويد بوهر معتقد بود که اتم مانند منظومه شمسی است. خورشید در مرکز قرار دارد و سیاره ها روی مدارهایی بدور خورشید در حال چرخش هستند در اتم نیز هسته در مرکز قرار دارد و الکترون هاروی مدارهایی دایره ای شکل با انرژیهای معین بدور هسته پیوسته در حال گردش هستند. |
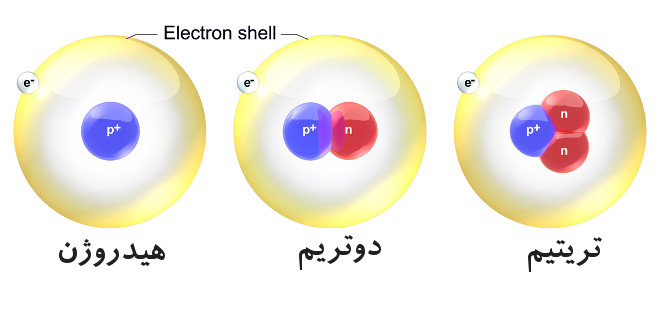
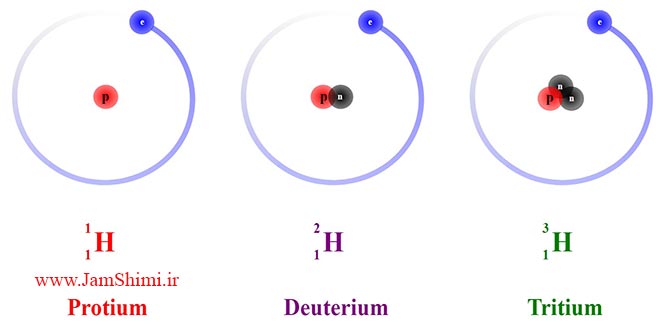
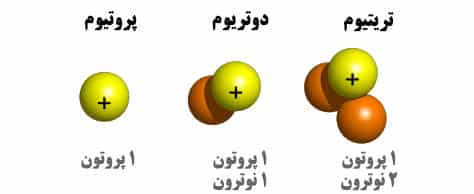
ایزوتوپ چیست؟ اتم هایی هستند که دارای عدداتمی یکسان می باشند ولی عدد جرمی متفاوت دارند. |  |
دلیل متفاوت بودن عدد جرمی در اتم های ایزوتوپی چیست؟ چون تعداد نوترون ها با هم متفاوت است.
|  |
|  |
نکته :
|  |
کاربردهای مفید مواد پرتوزا در زندگی روزمره عبارتند از:
|  |
هسته پرتوزا (رادیواکتیو) چیست؟
به هسته هایی گفته میشود که ناپایدار هستند و هنگام متلاشی شدن از خود پرتوهای پرانرژی و خطرناک پراکنده می کنند. مثل عنصر اورانیم - پلوتونیم | 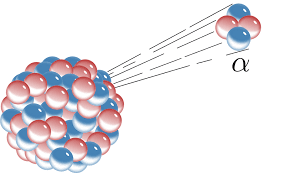 |
کاربرد مواد پرتوزا چیست؟
|  |
|  |
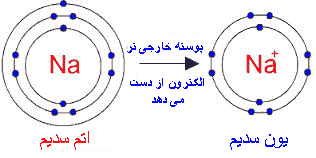
یون چیست ؟ ذره ای است که تعداد پروتون ها و الکترون هایش با هم برابر نیست. | 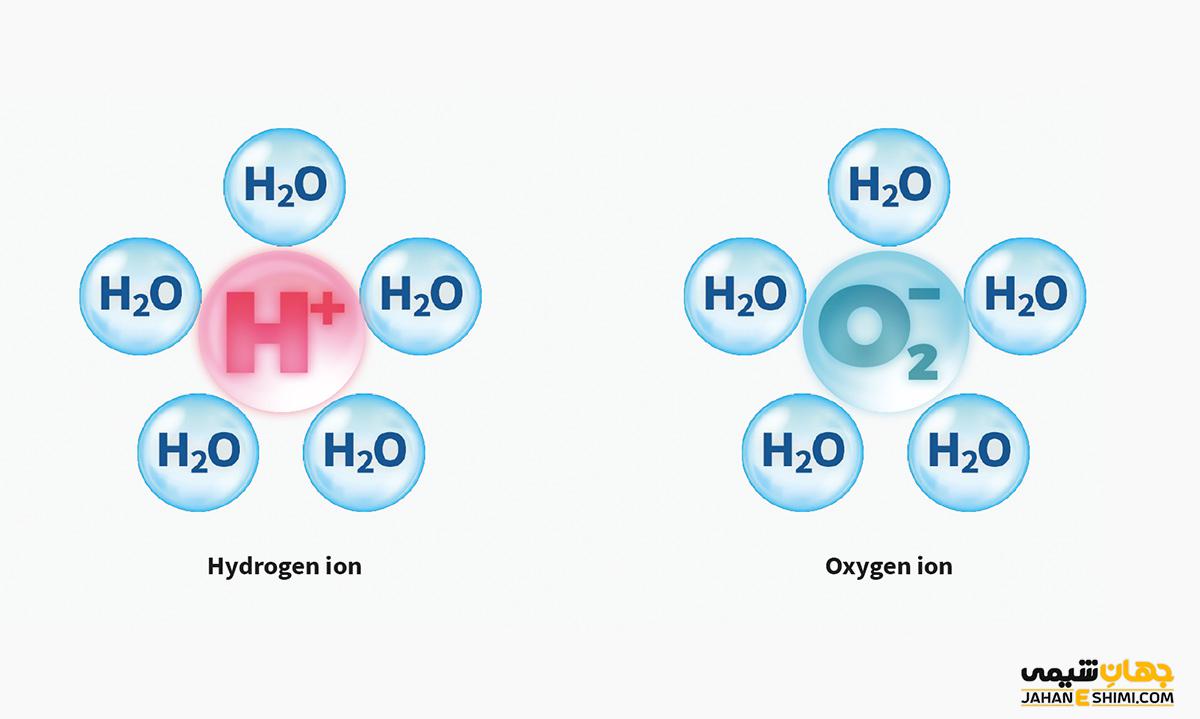 |
ترکیب یونی چیست؟ به ماده ای گفته می شود که ذرات سازنده آنها یون های (+) و (-) می باشند. |
ویژگی ترکیبات یونی عبارتند از:
| 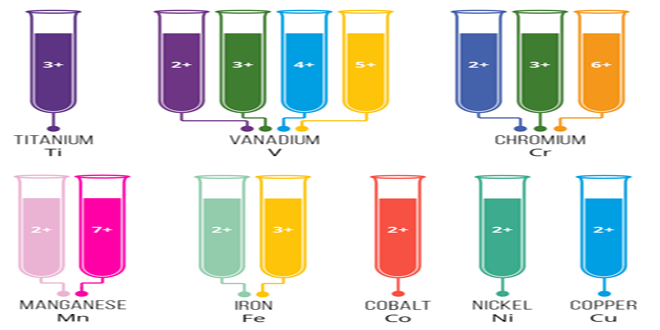 |
و حالا وقت تسته!!!
پاسخ تست ها در فایل ضمیمه قرار گرفته است.

برای ارتباط با پشتیبان ویژه و اطلاع از شرایط مشاوره با رتبه هاي برتركانوني
به لينك زير مراجعه كنيد.