سلام
در این مطلب میخواهیم با هم به جمع بندی نکات فصل 1 از صفحه 18 تا 48 (مطابق با آزمون جامع) و خلاصه نکات که برای پاسخگویی به سوالات آزمون باید به آنها مسلط باشید، بپردازیم.
مقایسه ی واکنش پذیری عناصر
واکنش پذیری هر عنصر به معنای تمایل اتم آن به انجام واکنش شیمیایی است.
هر چه واکنش پذیری اتمهای عنصری بیشتر باشد، در شرایط یکسان تمایل آن برای انجام واکنش و تبدیل شدن به ترکیب بیشتر است.
در هر واکنش شیمیایی که به طور طبیعی انجام می شود، واکنش پذیری فراورده ها از واکنش دهنده ها کمتر است؛ پس اگر یک واکنش به ما بدهند که در دو طرفش به عنصر آزاد وجود داشته باشد و بگن که این واکنش به طور طبیعی انجام میشه، ما خیلی سریع می تونیم واکنش پذیری دو عنصر آزاد در دو طرف معادله را با هم مقایسه کنیم:
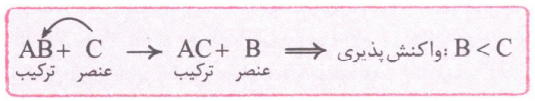
در معادله کلی بالا، واکنش پذیری C از B بیشتر بوده است؛ به همین دلیل میل بیشتری به تشکیل ترکیب داشته؛ از این رو با انجام واکنش، جاش رو با B عوض می کند. واکنش زیر به طور طبیعی انجام می شود.
هرچه واکنش پذیری فلز بیشتر باشد، در هوای مرطوب سریع تر واکنش می دهد.
تامین شرایط نگه داری برای سدیم و پتاسیم دشوارتر از بقیه ی فلز هاست چون تمایل به ایجاد ترکیب دارند.
به طور کلی در هر واکنش شیمیایی که به طور طبیعی انجام می شود، واکنش پذیری فرآورده ها از واکنش دهنده ها کم تر است.
به مقدار فرآورده مورد انتظار در هر واکنش، مقدار نظری و به مقدار فرآورده ای که در عمل تولید می شود، مقدار عملی گفته می شود.
کربن
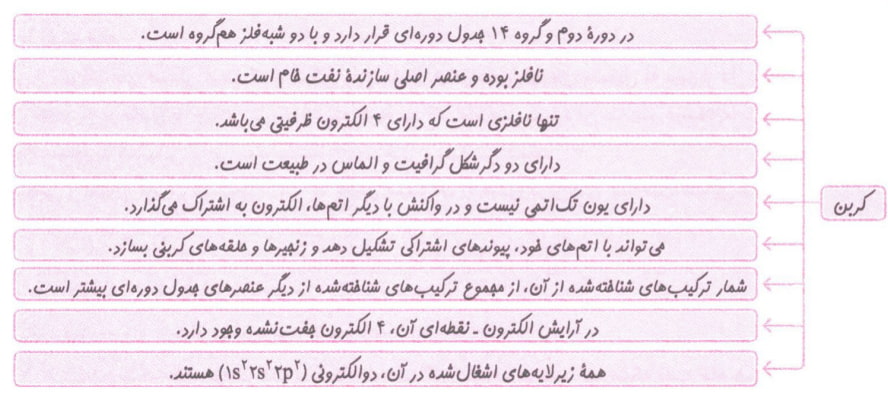

آلکان ها
آلکان ها دسته ای از هیدروکربن ها هستند ک در آن ها هر اتم کربن با چهار پیوند یگانه به اتم های اطراف متصل شده است. فرمول عمومی آنها به صورت CnH2n+2می باشد و جرم مولی آن ها از رابطه 14n+2 به دست می آید.
آلکان ها به دلیل داشتن پیوند های یگانه، تمایلی به انجام واکنش ندارند و سیر شده هستند و گشتاور دو قطبی آن ها حدود صفر است.
تجربه نشان می دهد که گشتاور دوقطبی آلکان ها حدود صفر است. بنابراین ناقطبی بوده و در آب نامحلول اند.
این ویژگی باعث می شود از آن ها برای حفاظت از فلزها استفاده شود. به این ترتیب که فلزها را در آلکان های مایع قرار می دهند و یا سطح فلزها را با آلکان ها، اندود می کنند تا از خوردگی فلز جلوگیری شود.
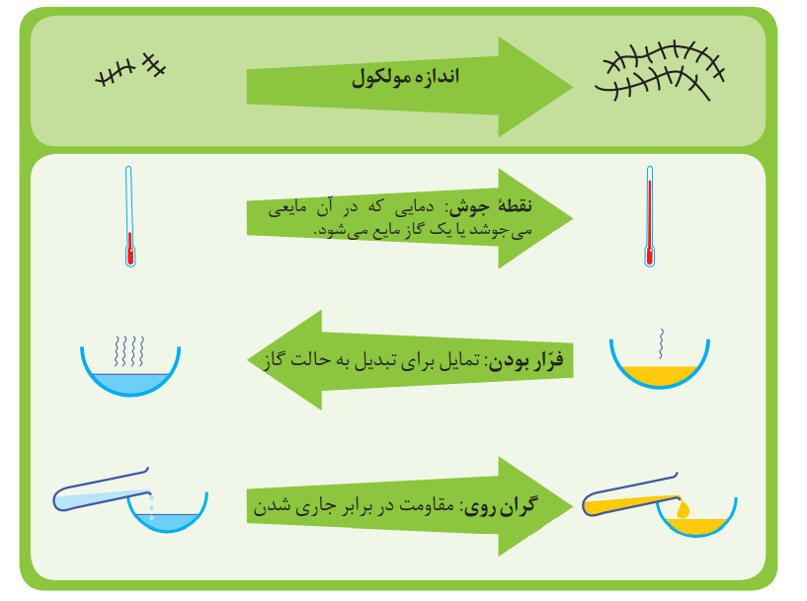
نقطه جوش
به طور کلی با افزایش تعداد اتم هایکربن و افزایش جرم مولی آن ها نیروی بین مولکولی که از نوع واندروالسی است، قوی تر شده و نقطه جوش افزایش می یابد.
فراربودن
به طور کلی هرچه نقطه جوش پایین تر باشد میزان فرار بودن آلکان ها نیز بیشتر است. بنابراین هرچه تعداد اتم های کربن کمتر باشد (جرم مولی کمتر)، فرار بودن آلکان بیشتر است.
گران روی
به طور کلی هر چه تعداد اتم های کربن در آلکان ها بیشتر باشد، گران روی آلکان نیز بیش تر است.
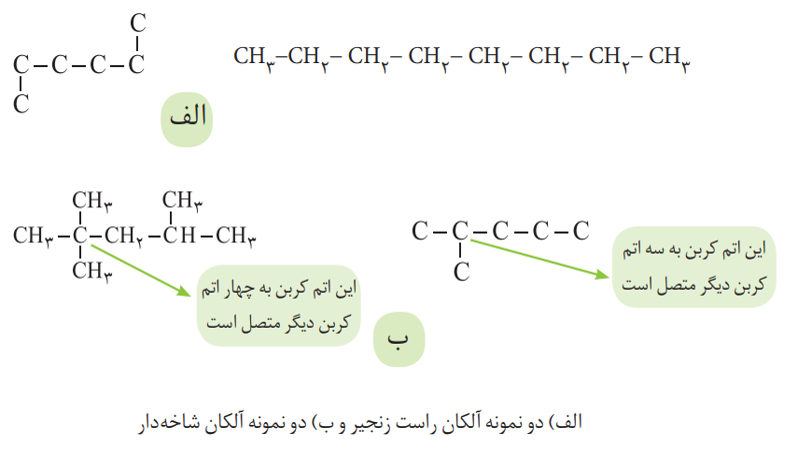
آلکان ها با توجه به نحوه قرار گرفتن اتم های کربن موجود در آن ها به دو دسته زیر تقسیم می شوند:
1- آلکان ها راست زنجیر: در این نوع آلکان ها، هر اتم کربن به یک یا دو اتم کربن دیگر متصل شده است.
2- آلکان های شاخه دار: در این آلکان ها، برخی کربن ها به سه یا چهار اتم کربن دیگر متصل اند.
آلکیل ها
اگر یک اتم H از فرمول آلکان ها کم کنیم گروهی جدیدی به نام آلکیل ها با فرمول CnH2n+1 به دست می آید. مانند متیل (CH3) و اتیل (C2H5)
آلکن ها
این هیدروکربن ها در ساختار خود دارای پیوند دوگانه کربن – کربن هستند. فرمول عمومی آن ها به صورت CnH2n می باشد و جرم مولی آن ها از رابطه 14n به دست می آید.
نام و ساختار چند آلکان راست زنجیر
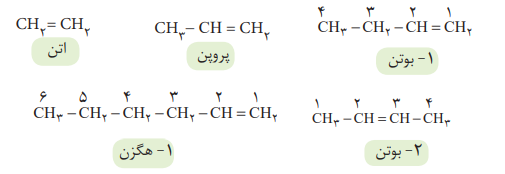
الف) واکنش آلکن ها با آب: در این واکنش الکل تولید می شود. به عنوان مثال با وارد کردن گاز اتن در مخلوط آب و اسید در شرایط مناسب، اتانول (الکل دو کربنه) در مقیاس صنعتی تولید می شود.
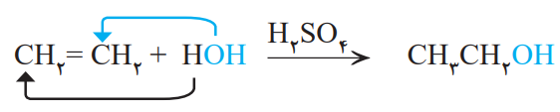
ب) واکنش آلکن ها با برم مایع: در این واکنش، پیوند دوگانه میان کربن ها شکسته و دو پیوند جدید بین اتم های کربن و اتم های کربن و اتم های Br (برم) ایجاد می شود. به عنوان مثال بر اثر واکنش برم مایع با گاز اتن، ترکیب سیر شده 2،1-دی برومو اتان به دست می آید.
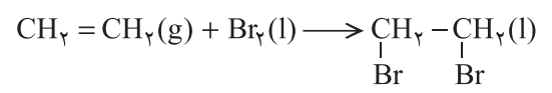
پ)پلیمر شدن آلکان ها: این واکنش ها در فصل سوم مورد بررسی قرار می گیرند که برای تولید انواع لاستیک ها، پلاستیک ها و الیاف به کار می رود.
ت)واکنش آلکن با گاز هیدروژن: در این واکنش آلکن ها با گاز هیدروژن در حضور کاتالیزگر نیکل واکنش داده و به آلکان تبدیل می شود. مانند:
آلکین ها از آلکان های هم کربن، 4 اتم هیدروژن کم تر و از آلکن های هم کربن، 2 اتم هیدروژن کم تر دارند. پس سیر نشده محسوب می شوند. البته واکنش پذیری آن ها از آلکن ها بیش تر است، چون سیر نشده تر از آلکن ها هستند.
آلکان < آلکن < آلکین :واکنش پذیری
هیدرو کربن های حلقوی
ترکیب های آلی بسیاری شناخته شده اند که در آن ها از اتصال 3 کربن، ساختاری حلقوی به وجود می آید.
هیدروکربن های حلقوی می توانند سیر شده یا سیر نشده باشند. به عنوان مثال سیکلو آلکان ها، سیرشده و ترکیبات آروماتیک سیر نشده می باشند.
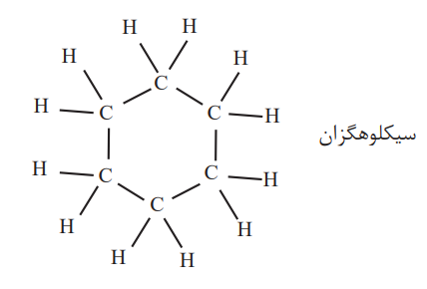
سیکلوآلکان ها: هیدروکربن های حلقوی سیر شده ای هستند که فرمول عمومی آن ها CnH2n می باشد. در آن ها ... و 4 و 3= n است.
هیدروکربن های آروماتیک: هیدروکربن های حلقوی سیر نشده ای هستند که بنزن سرگروه آن ها می باشد و دارای ساختار زیر است.
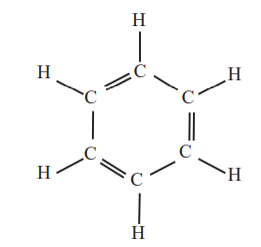
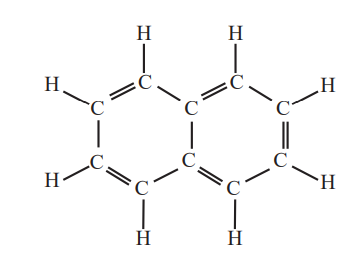
نفتالن: یکی دیگر از ترکیبات آروماتیک است که دارای فرمول مولکولی C10H8 می باشد. در این ترکیب پنج پیوند دوگانه یکی در میان و دو حلقه شش ضلعی وجود دارد.
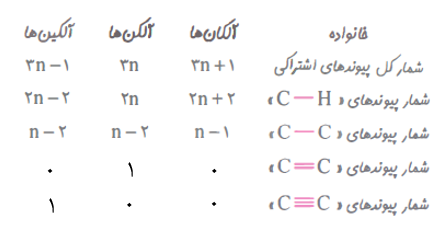
جمع بندی
تست های منتخب؛ (تست های زیر را حل کنید و پاسخ آن ها را در کامنت ها به اشتراک بگذارید!)
تست 1

تست 2

تست 3

تست 4
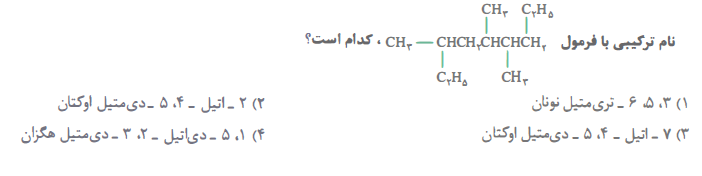
تست 5
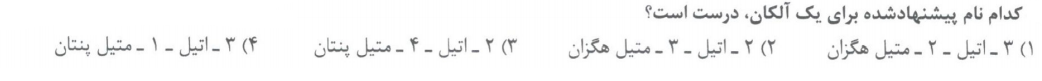
تست 6

تست 7

دوستان عزیز می توانید برای دسترسی به نسخه کامل خلاصه نکات به همراه پاسخ فایل پی دی اف زیر را دانلود کنید!
فراموش نکنید اگر سوالی در رابطه با این مبحث داشتید می توانید به راحتی در کامنت ها سوال خود را برای ما بنویسید.
دوستان عزیزم ما تصمیم گرفتیم برای اینکه بتونیم ارتباطمون رو با هم بیشتر کنیم و قدم به قدم کنارتون باشیم، صفحه ی اینستاگرام متا رو بسازیم
و همراهتون باشیم.
با آرزوی موفقیت و کامیابی
گلنوش بیرانوند، دانشجوی مهندسی شیمی دانشگاه شریف
نوید آرمات، دانشجوی مهندسی عمران دانشگاه تهران


