سلام
در این مطلب میخواهیم با هم به جمع بندی نکات موازنه واکنش و خواص و رفتار گاز ها شیمی دهم (مطابق با آزمون 31 اردیبهشت) و خلاصه نکات که برای پاسخگویی به سوالات آزمون باید به آنها مسلط باشید، بپردازیم.
نمایش واکنش های شیمیایی
تغییر شیمیایی تغییری است که با تغییر در ساختار و ماهیت مواد همراه است و ماده یا مواد جدیدی تولید می کند این نوع تغییر با تغییر رنگ،مزه، بو و آزاد سازی گاز، رسوب و گاهی ایجاد نور و صدا همراه است.به عنوان مثال گرما دادن به شکر سبب تغییر رنگ آن می شود. سوختن، فساد مواد غذایی و... نمونه هایی دیگر از تغییرات شیمیایی هستند.

سوخت سبز، سوختی است كه در ساختار خود افزون بر كربن و هیدروژن، اكسیژن نیز دارد و از پسماندهای گیاهی مانند شاخ و برگ گیاه سویا، نیشكر و دانه های روغنی به دست می آید.این مواد زیست تخریب پذیرند، از این روبه وسیله ی جانداران ذره بینی به مواد ساده تر تجزیه می شوند. اتانول و روغن های گیاهی نمونه هایی ازاین نوع سوخت ها هستند.
شیمی سبز:
1-تولید سوخت سبز 2- تبدیلCO2 به مواد معدنی
3-تولید پلاستیک های سبز 4-دفن کردن کربن دی اکسید
5- تولید خودرو و سوخت با کیفیت بسیار خوب
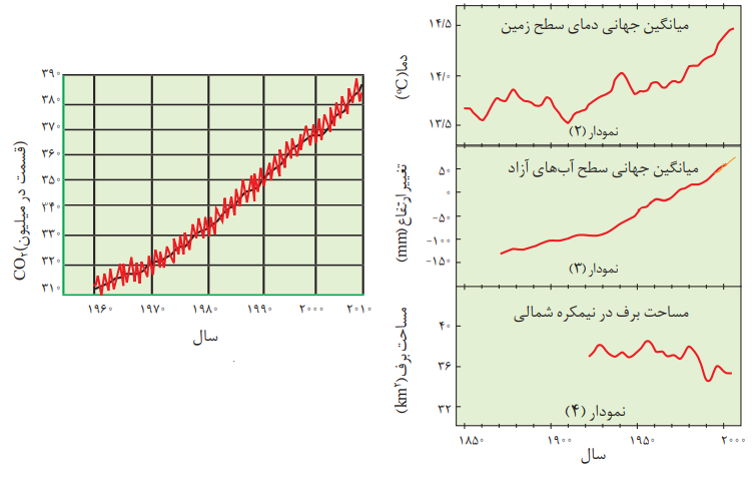
ردپای کربن دی اکسید و اثر گلخانه ای وجود گازهای گلخانه ای مانند CO2 سبب ایجاد اثر گلخانه ای می شود. این افزایش دما سبب ذوب شدن بیش تر برف ها و یخچال هاو در نهایت افزایش میانگین جهانی سطح آب های آزاد می شود.
افزایش میانگین جهانی دماس سطح زمین سبب شده تا فصل بهار در نیمکره شمالی زمین، نسبت به 50 سال گذشته در حدود یک هفته زودتر آغاز شود.

خواص و رفتار گازها:
1- رابطه بین فشار و حجم گاز:
بهطور کلی برای مقدار مشخصی گاز در دمای ثابت، حجم گاز با فشار آن رابطه عکس دارد.(قانون بویل)
2- رابطه بین دما و حجم گازها:
بهطور کلی در فشار ثابت، دمای گازها باحجم آن ها رابطه ی مستقیم دارد. (قانون شارل). بنابراین اگر مقدار معینی از گاز بافشار معین را گرم کنیم حجم آن بیش تر خواهد شد و بالعکس.
3- رابطه بین مول و حجم گازها (قانون آووگادرو)
بهطور کلی در دما و فشار ثابت،حجم هر گازی به تعداد مول های آنبستگی دارد. بنابراین می توان گفت حجم یک مول از گازهای گوناگون در دما و فشاریکسان با هم برابر است. (قانون آووگادرو)
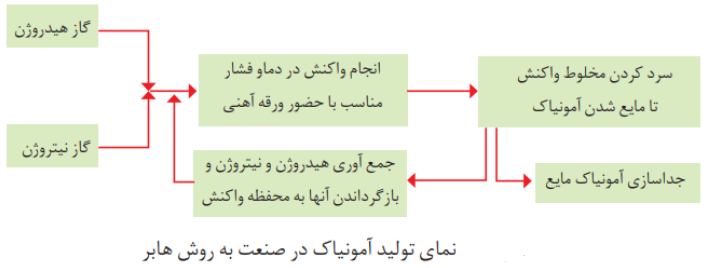
فرآیند هابر
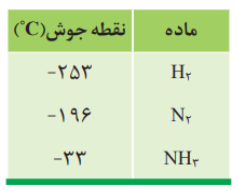
هابر واكنش میان گازهای هیدروژن و نیتروژن را بارها در دماها و فشارهای گوناگون انجام داد تا بتواند شرایط بهینه آن راپیدا كند. سرانجام دریافت که اگر مخلوط این گازها از روی یك ورقه ی آهنی (کاتالیزگر) در دما و فشار مناسب عبور داده شود با انجام واكنش، مقدار قابل توجهی آمونیاك تولید می شود؛ اما همه ی واكنش دهنده ها به فرآورده تبدیل نخواهد شد؛ زیرا این واكنش برگشت پذیر است؛ با این توصیف در ظرف واكنش مخلوطی از سه گاز هیدروژن، نیتروژن و آمونیاك وجود دارد.
دوستان عزیز می توانید برای دسترسی به نسخه کامل خلاصه نکات به همراه پاسخ فایل پی دی اف زیر را دانلود کنید!
فراموش نکنید اگر سوالی در رابطه با این مبحث داشتید می توانید به راحتی در کامنت ها سوال خود را برای ما بنویسید.
دوستان عزیزم ما تصمیم گرفتیم برای اینکه بتونیم ارتباطمون رو با هم بیشتر کنیم و قدم به قدم کنارتون باشیم، صفحه ی اینستاگرام متا رو بسازیم
و همراهتون باشیم.
با آرزوی موفقیت و کامیابی
گلنوش بیرانوند، دانشجوی مهندسی شیمی دانشگاه شریف
نوید آرمات، دانشجوی مهندسی عمران دانشگاه تهران


