سلام
در این مطلب میخواهیم با هم به جمع بندی نکات شیمی 2 از صفحه 12 تا 17 (مطابق با آزمون) و خلاصه نکات که برای پاسخگویی به سوالات آزمون باید به آنها مسلط باشید، بپردازیم.
نوید آرمات، دانشجوی مهندسی عمران دانشگاه تهران
سیده محدثه حسینی، دانشجوی دکتری تخصصی پیوسته بیوتکنولوژی دانشگاه تهران
شعاع اتمی
به طور کلی هر چه شعاع یک اتم بزرگتر باشد، اندازه آن اتم نیز، بزرگتر است.
به طورکلی، شعاع اتمی عنصرهای جدول دوره ای در یک گروه از بالا به پایین افزایش می یابد؛ زیرا تعداد لایه های الکترونی بیش تر می شود.
به طور کلی در یک دوره شعاع اتمی از چپ به راست کاهش می یابد؛ زیرا در یک دوره تعداد لایه های الکترونی ثابت می ماند؛ در حالی که تعداد پروتون های هسته بر الکترون ها بیش تر شده و شعاع اتم کاهش می یابد.
در بین تمام عناصر جدول دوره ای، عنصر Fr دارای بیش ترین و عنصر H دارای کم ترین شعاع اتمی است.
توجه: از آن جا که عنصر Fr بسیار کمیاب است، می توان شعاع Cs رابه عنوان بیش ترین شعاع اتمی در نظر گرفت.
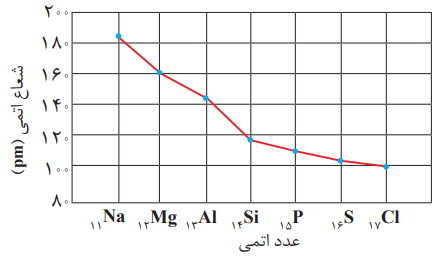 دراین دوره بیشترین تفاوت شعاع اتمی دو عنصر متوالی به Si , Al مربوط است.
دراین دوره بیشترین تفاوت شعاع اتمی دو عنصر متوالی به Si , Al مربوط است.با توجه به نمودار می توان فهمید که شیب تغییرات شعاع در ابتدا (سمت چپ) تناوب بیش تر از شیب آن ها در انتها (سمت راست) تناوب است که این موضوع به دلیل افزایش دافعه بین الکترون ها در عناصر انتهایی تناوب می باشد.
با توجه به روند تغییر شعاع اتمی در یک گروه و دوره، هر چه عنصری در جدول دوره ای، سمت چپ تر و پایین تر، شعاع آن بزرگتر است و بالعکس.
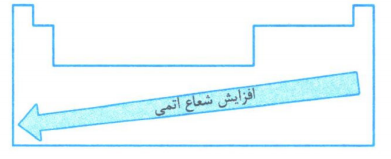
رابطه خصلت فلزی و نافلزی با شعاع اتم ها
هر چه شعاع اتم بزرگتر اتم آسان تر الکترون از دست می دهد و خصلت فلزی افزایش می یابد.
خصلت فلزی عناصر گروه اول از عناصر هم دوره گروه دوم بیش تر است که این موضوع به دلیل کم تر بودن تعداد الکترون ظرفیت عناصر گروه اول (1 الکترون) نسبت به تعداد الکترون های لایه ظرفیت گروه دوم (2 الکترون) می باشد.
به طور کلی هر چه شعاع اتمی کوچک تر می شود، اتم آسان تر الکترون می گیرد، بنابراین دلیل اینکه خصلت نافلزی در یک گروه از بالا به پایین کاهش می یابد، افزایش شعاع اتم می باشد.

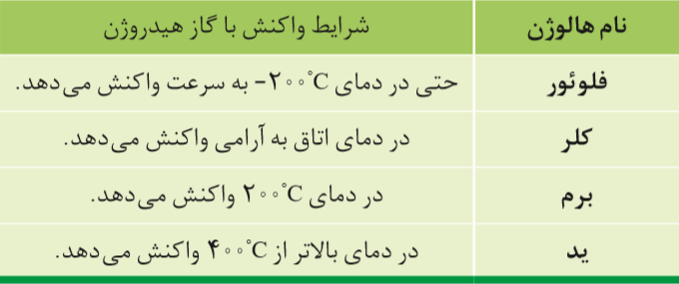
فلزات واسطه
دسته ای از عناصر جدول دوره ای می باشند که در مرکز جدول دوره ای قرار دارند و زیر لایه d در آن ها در حال پر شدن است و دارای خصوصیات زیر هستند:
1- همگی فلز هستند و دارای رسانایی الکتریکی و گرمایی می باشند.
2- اغلب این فلز ها در طبیعت به شکل ترکیب های یونی مانند اکسیدها، کربنات ها و .... یافت می شوند.
3- یون های فلزات واسطه و ترکیبات یونی دارای این یون ها اغلب رنگی هستند. به عنوان مثال یون مس 󠄤∏، آبی رنگ است.
4- مهم ترین فلزات واسطه مربوط به دوره ی چهارم جدول دوره ای هستند که عدد اتمی آن ها 21 تا 30 می باشد.
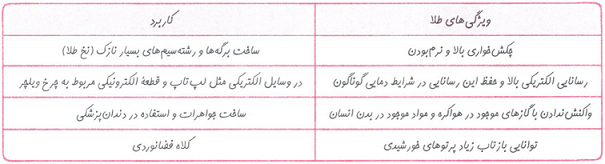
طلا 79Au فلزی ارزشمند و گران از دسته ی d جدول دوره ای است که علاوه بر علاوه بر ویژگی های مشترک فلزها، ویژگی های منحصر به فردی دارد.
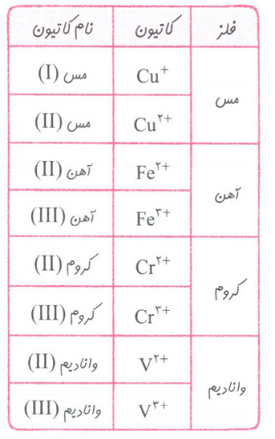
برخی از فلزهای واسطه که بیش ازیک نوع کاتیون دارند.
تست 1:

تست 2:

دوستان عزیز می توانید برای دسترسی به نسخه کامل خلاصه نکات به همراه پاسخ فایل پی دی اف زیر را دانلود کنید!
فراموش نکنید اگر سوالی در رابطه با این مبحث داشتید می توانید به راحتی در کامنت ها سوال خود را برای ما بنویسید.
دوستان عزیزم؛ برای ارتباط با رتبه برترها صفحه اینستاگرام زیر رو دنبال کنید.
با آرزوی موفقیت و کامیابی


