سلام
در این مطلب میخواهیم با هم به جمع بندی فصل دوم شیمی یازدهم و هم چنین خلاصه نکاتی که برای پاسخگویی به سوالات آزمون باید به آنها مسلط باشید، بپردازیم.
نقش غذا در بدن علاوه بر رفع گرسنگی به صورت زیر است:
1-تامین انرژی مورد نیاز برای حرکت ماهیچه ها، ارسال پیام عصبی، جا به جایی یون ها ومولکول ها از دیواره ی سلولی
2-ماده ی اولیه برای ساخت و رشد بخش های گوناگون بدن مانند سلول های خونی، استخوان، پوست، مو، ماهیچه ها، آنزیم ها و...
دمای ماده از چه خبر می دهد؟
دما کمیتی است که میزان گرمی و سردی مواد را نشان می دهد. از دیدگاه ذره ای، ذره های سازنده ی ماده همواره در حال جنب و جوش هستند. اما در حالت های فیزیکی متفاوت، میزان جنبش ذرات متفاوت از یکدیگر است.
نکته: به طور کلی این جنبش های نامنظم درحالت گاز شدیدتر از مایع و در حالت مایع نیز شدیدتر از حالت جامد است.
تفاوت دما و گرما
به طور کلی به مقدار انرژی گرمایی که به دلیل تفاوت در دما جاری می شود گرما گفته می شود که با نماد (Q) نشان داده می شود و یکای اندازه گیری آن در «SI» ژول (J) است. البته هنوز در برخی موارد از کالری (cal) برای بیان مقدار گرما استفاده می شود.
فرآیندهای گرماده: در این فرآیند ها انرژی به صورت گرما از سامانه به محیط جاری می شود و دمای سامانه کاهش می یابد. Q<0
فرآیندهای گرماگیر: در این نوع فرآیند ها انرژی به صورت گرما از محیط به سامانه منتقل می شود و دمای سامانه افزایش می یابد. Q>0
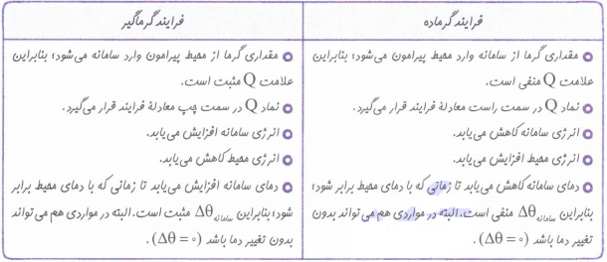
نکته:ممکن است در فرآیند های گرماگیر و گرماده دما بدون تغییر باقی بماند.
مفهوم آنتالپی:
انرژی کل یک سامانه هم ارز با محتوی انرژی یا آنتالپی آن می باشد. بنابراین هر سامانه در دما و فشار ثابت آنتالپی معینی دارد.
در واکنش های گرماگیر مواد با آنتالپی کم تر به مواد با آنتالپی بیش تر تبدیل می شوند.
در واکنش های گرماده مواد با آنتالپی بیش تر به مواد با آنتالپی کم تر تبدیل می شوند.
نکته: آنتالپی پیوند های متفاوت به دو عامل وابسته است:
1) مرتبه پیوند (تعداد پیوند های بین دو اتم): هر چه مرتبه پیوند بیش تر باشد، انرژی پیوند بیش تر است.
2)شعاع اتم های تشکیل دهنده پیوند: هرچه شعاع اتم های تشکیل دهنده پیوند بیش تر باشد، آنتالپی پیوند کوچک تر است.
نکته: همچنین در یک پیوند هرچه اختلاف الکترونگاتیوی بین دو اتم بیش تر باشد قطبیت پیوند بیش تر شده و جاذبه بین دو اتم قوی تر می شود لذا انرژی پیوند افزایش می یابد.
آنتالپی سوختن:
سوختن تغییر شیمیایی است که طی آن یک ماده به سرعت واکنش می دهد و انرژی زیادی به صورت گرما آزاد می کند. آنتالپی واکنشی را که در آن یک مول از ماده در مقدار اکسیژن کافی بسوزد، آنتالپی سوختن آن ماده می نامند که دارای واحد کیلوژول بر مول و علامت منفی است.
نکته: یکی از فرآورده های سوختن مواد آلی به صورت H2O است که به صورت مایع است.
نکته: هرچه جرم هیدروکربنی بیش تر باشد، گرمای حاصل از سوختن آن بیش تر است.
نکته: گرمای حاصل از سوختن آلکان ها از الکل های هم کربن خودشان بیش تر است.
گروه های عاملی مهم اکسیژن دار
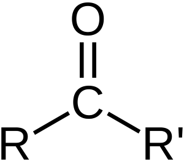
گروه کربونیل
این گروه عاملی مختص آلدهید ها و کتون هاست. در آلدهید ها این گروه عاملی در ابتدای زنجیره کربنی قرار می گیرد و از یک سمت حتما به H متصل است. مانند بنزآلدهید. ولی درکتون ها این گروه عاملی از هر دو سمت به کربن متصل است.
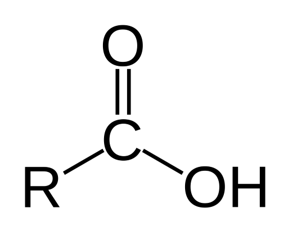
گروه هیدروکسیل
این گروه عاملی مختص الکل ها است. مانند ترکیب آلی موجود در گشنیز که سبب طعم و بوی آن می شود.
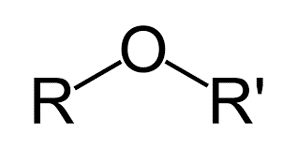
گروه اتری
این گروه مختص اتر هاست. مانند ترکیب آلی موجود در رازیانه که موجب ایجاد طعم و بوی آن می شود.
ایزومر
به موادی که فرمول مولکولی یکسان ولی ساختار متفاوتی دارند، ایزومر یا هم پار گفته می شود.
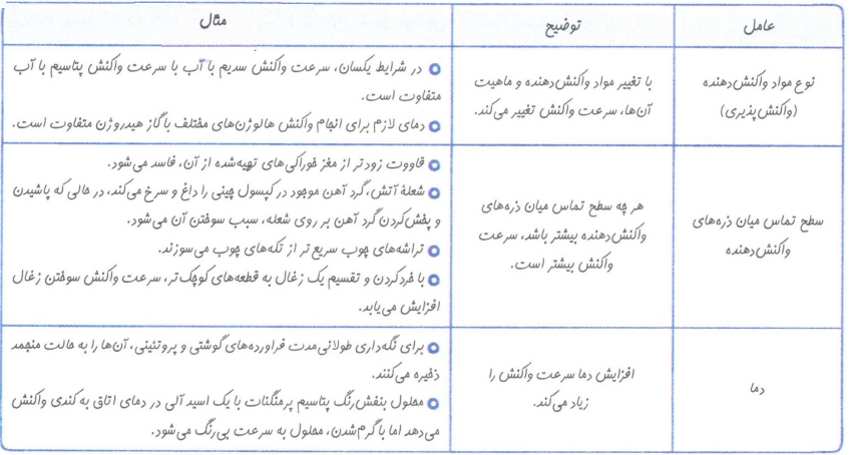
نکته: سرعت انجام واکنش به نوع مواد واکنش دهنده، سطح تماس واکنش دهنده ها، غلظت واکنش دهنده ها، دما و کاتالیزگر وابسته است.
نکته:کاتالیزگر ماده ای است که سرعت واکنش شیمیایی را افزایش می دهند ولی خود مصرف نمی شود. مثلا حضور کاتالیزگر KI سبب تسریع تجزیه شدن هیدورژن پراکسید در دمای اتاق می شود.
نکته:هرچه سطح جامدات کوچک تر باشد سرعت انجام واکنش بیش تر است.
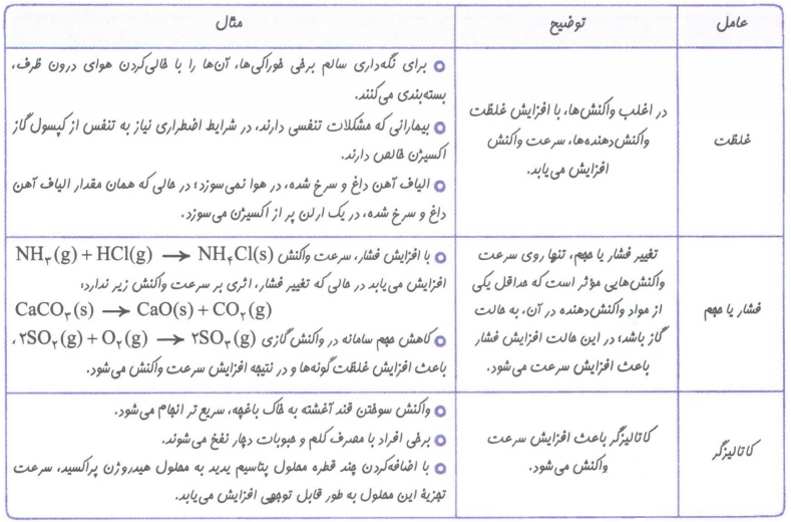
نکته:در برخی واکنش های تغییر غلظت تاثیری بر سرعت واکنش ندارد.
نکته:در واکنش هایی که حداقل یکی از واکنش دهنده ها گازی باشد تغییر فشار، سرعت انجام واکنش را تغییر خواهد داد.
نکته:افزایش دما سبب افزایش انرژی ذرات و طبیعتا افزایش سرعت انجام واکنش می شود.
نکته:افزودن کاتالیزگر سبب افزایش مقدار فرآورده نمی شود بلکه همان مقدار فرآورده با سرعت بیش تر و در زمان کوتاه تری تولید می شود.
نکته:نگهدارنده ها سرعت واکنش های شیمیایی را که منجر به فساد می شود، کاهش می دهند. یکی از این مواد بنزوییک اسید است که در توت فرنگی و تمشک موجود است.
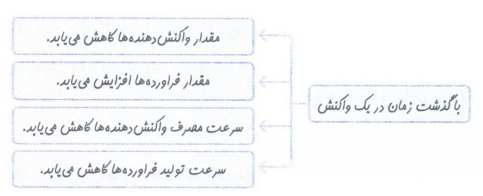
تست های منتخب؛ (تست های زیر را حل کنید و پاسخ آن ها را در کامنت ها به اشتراک بگذارید!)
تست 1

تست 2

تست 3

تست 4

تست 5

تست 6
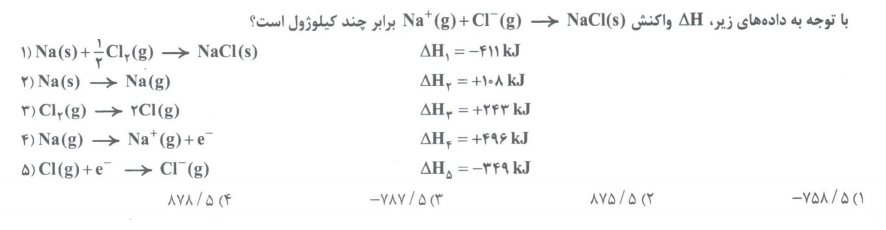
تست 7

دوستان عزیز می توانید برای دسترسی به نسخه کامل خلاصه نکات به همراه پاسخ فایل پی دی اف زیر را دانلود کنید!
فراموش نکنید اگر سوالی در رابطه با این مبحث داشتید می توانید به راحتی در کامنت ها سوال خود را برای ما بنویسید.
دوستان عزیزم ما تصمیم گرفتیم برای اینکه بتونیم ارتباطمون رو با هم بیشتر کنیم و قدم به قدم کنارتون باشیم، صفحه ی اینستاگرام متا رو بسازیم
و همراهتون باشیم.
با آرزوی موفقیت و کامیابی
الهه پروری، فارغ التحصیل مهندسی شیمی دانشگاه تهران
نوید آرمات، دانشجوی مهندسی عمران دانشگاه تهران


